
设NA为阿伏加德罗常数的值.下列说法正确的是( )
A.1.6gNH2-和1.5g—CH3含有的电子数均为NA
B.标准状况下,将2.24L 氯化氢溶于足量水中,溶液中含有的HCl分子数为0.1NA
C.氢氧化钠溶于与氯气反应时,生成0.1molNaCl转移的电子数为0.1NA
D.12gNaHSO4晶体中阳离子和阴离子的总数为0.3NA
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:填空题
某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下步骤进行:
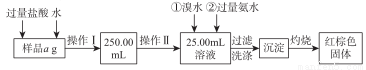
请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 。 (填仪器名称)
(2)请写出加入溴水发生的离子反应方程式 。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g。再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是 。若蒸发皿质量是 W1 g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是 。有同学提出,还可以采用以下方法来测定:
①溶解样品改用了硫酸,而不用盐酸,为什么 。
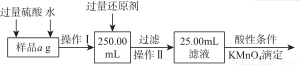
②选择的还原剂是否能用铁 (填“是”或“否”),原因是: 。
③若滴定用掉c mol/ L KMnO4溶液bmL,则样品中铁元素的质量分数是 。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前预测化学试卷(解析版) 题型:推断题
异苯丙醛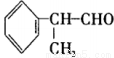 在工业上有重要用途,其合成流程如下:
在工业上有重要用途,其合成流程如下:
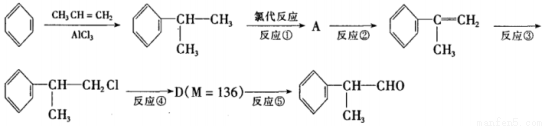
(1)异苯丙醛被酸性高锰酸钾氧化后所得有机物的结构简式是____________。
(2)在合成流程上②的反应类型是____________,反应④发生的条件是____________,
(3)反应⑤的化学方程式为____________。
(4)异苯丙醛发生银镜反应的化学方程式为__________。
(5)D物质与有机物X在一定条件下可生成一种相对分子质量为178的酯类物质,则X的名称是____________。D物质有多种同分异构体,其中满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有____________种。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前预测化学试卷(解析版) 题型:选择题
某学生对碱性工业废水样品进行研究,其实验操作或结论的描述,正确的是( )
A.将废水加入紫色石蕊试剂中检验酸碱性
B.用玻璃棒蘸取废水样品,蘸在润湿的pH试纸上测定其pH
C.测得该废水样品的pH=10,则废水样品中c(OH-)=10-10mol/L
D.该工业废水中c(H+)<c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三第八次月考理综化学试卷(解析版) 题型:推断题
已知 X、Y、U、V、W、Z是六种常见元素,其中X、Y、U、V、W五种短周期元素在周期表中的位置如图所示:U的最简单气态氢化物能使湿润的红色石蕊试纸变蓝.Z是人体血红蛋白中存在的金属元素.请回答下列问题:
Y | U | |||
X | V | W |
(1)Z元素在周期表中的位置__________,ZW3的水溶液可以净水的原因是__________(用离子方程式、结合文字说明)
(2)X、U、V、W形成的简单离子半径由大到小的顺序为__________(用离子符号表示)
(3)若将少量U的最简单氢化物与过量W的单质混合,则生成一种酸和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式__________,A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式__________。
(4)二氧化钛(TiO2)与X的单质、Y的单质高温下反应生成两种化合物,这两种化合物均由两种元素组成,其反应的化学方程式为__________,若有1molX的单质参加反应,转移的电子数目为__________。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三5月高考模拟理综化学试卷(解析版) 题型:实验题
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂.其制备工艺流程如图:

已知:反应II包含2NaHSO3═Na2S2O5+H2O等多步反应。
(1)反应I的总化学方程式为____________,反应I进行时应先通入的气体是____________,反应I产生的NH4Cl可用作____________。
(2)灼烧时发生反应的化学方程式为____________,若灼烧时生 成SO21.12×l06 L(标准状况下),则转移电子____________mol.
(3)己知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为____________;
(4)副产品X的化学式是____________,在上述流程中可循环使用的物质是____________;
(5)为了减少产品Na2S2O5中杂质含量,需控制反应II中气体与固体的物质的量之比约为____________,检验产品中含有碳酸钠杂质所需试剂____________(填编号).
①澄清石灰水 ②饱和碳酸氢钠溶液 ③氢氧化钠 ④酸性高锰酸钾 ⑤稀硫酸
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
常温下,0.2mol•L-1的一元酸HA与等浓度NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度所示,下列说法正确的是( )
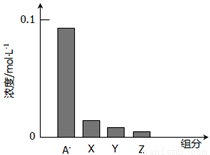
A.HA为强酸
B.该混合溶液pH=7.0
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二5月月考化学试卷(解析版) 题型:选择题
用黄色的FeCl3溶液分别进行下列实验,解释或结论不正确的是( )
实验 | 现象 | 解释或结论 | |
A | 加入FeCl3固体 | 溶液变成红褐色 | FeCl3的水解程度变大 |
B | 加入等体积水 | 溶液颜色变浅 | c(Fe3+)变小 |
C | 加入足量Fe粉 | 溶液颜色变浅绿色 | 2Fe3++Fe=3Fe2+ |
D | 将FeCl3溶液微热 | 溶液变成红褐色 | 水解反应△H>0 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:填空题
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示(a、b为石墨电极,不考虑U形管中气体的溶解且a上产生的气体全部进入小试管中)。
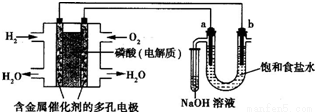
(1)写出通入H2这一极的电极反应_________,通入O2这一极的电极反应为_________。
(2)a为_________极,电极反应为_________ 。
(3)b为_________极,电极反应为_________。
(4)在25℃,当燃料电池中消耗 0.02g H2时,U形管中液体的体积为200mL(忽略实验过程中体积的变化), 求此时U形管中溶液的pH。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com