
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种。请根据所学化学知识回答下列问题:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中离子浓度由大到小的顺序为
________________________________________________________________________
________________________________________________________________________。
(2)B为0.1 mol·L-1的NaHCO3溶液,NaHCO3在该溶液中存在的平衡有(用离子方程式表
示)________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)C为0.1 mol·L-1的(NH4)2Fe(SO4)2溶液,与同浓度的(NH4)2SO4溶液相比较____________(填溶质的化学式)溶液中NH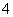 的浓度更大,其原因是
的浓度更大,其原因是
________________________________________________________________________
________________________________________________________________________。
(4)D为含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:AgCl(s)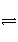
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在25℃时,AgCl的Ksp=1.8×10-10 mol2·L-2。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水
②100 mL 0.3 mol·L-1AgNO3溶液 ③100 mL 0.1 mol·L-1 MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为____________(填序号),此时溶液②中Cl-物质的量浓度为______________。
(1)[NH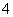 ]>[SO
]>[SO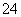 ]>[H+]>[OH-]
]>[H+]>[OH-]
(2)HCO
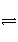
 H++CO
H++CO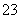 ;HCO
;HCO +H2O
+H2O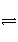
 H2CO3+OH-;H2O
H2CO3+OH-;H2O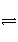
 H++OH-
H++OH-
(3)(NH4)2Fe(SO4)2 Fe2+水解显酸性,对NH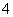 的水解有抑制作用
的水解有抑制作用
(4)②>①>③ 6×10-10 mol·L-1
解析 (1)NH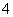 水解显酸性且水解程度小,所以有:
水解显酸性且水解程度小,所以有:
[NH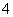 ]>[SO
]>[SO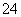 ]>[H+]>[OH-]。
]>[H+]>[OH-]。
(2)NaHCO3溶液中存在三个平衡体系:
①HCO 的电离平衡:HCO
的电离平衡:HCO
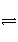
 H++CO
H++CO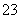 ;②HCO
;②HCO 的水解平衡:HCO
的水解平衡:HCO +H2O
+H2O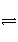
 H2CO3+OH-;③H2O的电离平衡:H2O
H2CO3+OH-;③H2O的电离平衡:H2O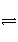
 H++OH-。
H++OH-。
(3)(NH4)2Fe(SO4)2溶液中,Fe2+水解产生的H+对NH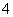 的水解起抑制作用,NH
的水解起抑制作用,NH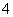 水解程度小,与同浓度的(NH4)2SO4溶液相比,前者NH
水解程度小,与同浓度的(NH4)2SO4溶液相比,前者NH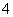 的浓度更大。
的浓度更大。
(4)①与③相比,③溶液中的Cl-使AgCl的溶解平衡逆向移动,[Ag+]最小,②中溶液中的Ag+虽然使AgCl的溶解平衡逆向移动,但溶液中Ag+的浓度要比①、③中Ag+的浓度大的多,所以②中Ag+浓度最大。②中[Cl-]=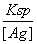 =
=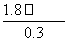 mol·L-1=6×10-10 mol·L-1。
mol·L-1=6×10-10 mol·L-1。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
“富勒烯”家族又增添了新成员,继C60、C70、N60之后,中美科学家首次发现了全硼富勒烯B40.下列说法正确的是
A. B40、C70都属于新型化合物 B. C60和N60属于同分异构体
C. B40、C60、C70、N60都属于烯烃 D. B40、C60、C70、N60都只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
已知硫酸亚铁溶液中加入过氧化钠时发生反应:
4Fe2++4Na2O2+6H2O= 4Fe(OH)3↓+O2↑+8Na+ 则下列说法正确的是( )
A、该反应中 Fe2+是还原剂,O2 是还原产物
B、4molNa2O2 在反应中共得到 8NA 的电子
C、Fe(OH)3 既是氧化产物又是还原产物,每生成 4mol Fe(OH)3 反应过程中共转移电子 6mol
D、反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某溶液中由水电离的[H+]=1×10-13 mol·L-1,该溶液可能是( )
①三氧化硫水溶液 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
电离常数(Ka或Kb)、溶度积常数(Ksp)是判断物质性质的重要常数,下列关于这些常数的计算或运用正确的是( )
A.某亚硫酸溶液pH=4.3,若忽略二级电离,则其一级电离平衡常数K1=1.0×10-8.60 mol2·L-2
B.Ka(HCN)<Ka(CH3COOH),说明同浓度时氢氰酸的酸性比醋酸强
C.Ksp(AgI)<Ksp(AgCl),向AgCl悬浊液中加入KI溶液会出现黄色沉淀
D.Ksp(AgCl)<Ksp(AgOH),说明AgOH和AgCl均不溶于稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
在苯的同系物中加入少量的酸性KMnO4溶液,振荡后褪色,正确的解释为( )
A.苯的同系物分子中的碳原子数比苯分子中的碳原子数多
B.苯环受侧链影响易被氧化
C.侧链受苯环影响易被氧化
D.由于苯环和侧链的相互影响均易被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A的分子式为C10H14,它不能使溴水褪色,但能使酸性KMnO4溶液褪色,经测定数据表明,分子中除含苯环外不再含有其他环状结构,且苯环上只有一个侧链,符合此条件的烃的结构有( )
A.3种 B.4种 C.5种 D.7种
查看答案和解析>>
科目:高中化学 来源: 题型:
已知(a、b分别代表不同的原子或原子团)互为同分异构体。 据此推断一氯丙烯的同分异构体 (不含环状结构)共有
A.3种 B.4种 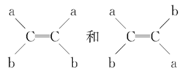
C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
乳酸(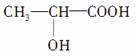 )自身可形成多种酯,请按相对分子质量由小到大的顺序________写出酯的结构简式____________________、____________________、
)自身可形成多种酯,请按相对分子质量由小到大的顺序________写出酯的结构简式____________________、____________________、
____________、____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com