
根据同分异构体的概念,判断下列物质互为同分异构体的是( )
A. CH3﹣CH2﹣NO2 和 H2N﹣CH2﹣COOH
B. H和D
C. 甲烷和正丁烷
D. 红磷和白磷
科目:高中化学 来源:广东省2016-2017学年高二上学期期末考试化学(文)试卷 题型:选择题
高温高压下,1 L密闭容器中,发生如下反应:2H2+CO  CH3OH ,反应开始时H2的物质的量为5 mol,5 min时变为0.5 mol,则5 min内该反应的平均反应速率
CH3OH ,反应开始时H2的物质的量为5 mol,5 min时变为0.5 mol,则5 min内该反应的平均反应速率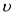 (H2) (单位:mol·L-1·min-1)为
(H2) (单位:mol·L-1·min-1)为
A. 9.0 B. 0.9 C. 0.45 D. 4.5
查看答案和解析>>
科目:高中化学 来源:2017届浙江省温州市高三第二次选考模拟考试(2月)化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. 蔗糖、棉花和蚕丝均为高分子化合物
B. 油脂是高级脂肪酸甘油酯,在氢氧化钠溶液中纾解完全后混合液出现分层
C. 淀粉在人体内淀粉酶的作用下得到葡萄糖,葡萄糖缓慢氧化,放出热量提供生命活动所需要的能量
D. 王鸡蛋清的溶液中加入饱和硫酸铵溶液,可观察到蛋白质发生凝聚,再加入蒸馏水,振荡后蛋白质不溶解
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高二下学期期初化学试卷 题型:实验题
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图:
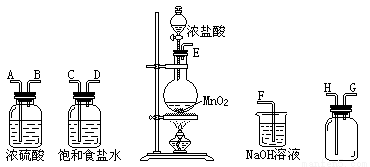
(1)连接上述仪器的正确顺序是:E接 , 接 , 接 , 接F.____________
(2)气体发生装置中进行的反应化学方程式是_________________;当0.5mol MnO2参与反应时,被氧化的HCl的质量为____________,生成的Cl2在标准状况下的体积约为____________.
(3)在装置中:①饱和食盐水的作用是______________,②浓硫酸的作用是__________.
(4)化学实验中检验是否有Cl2产生常用湿润的淀粉﹣KI试纸.如果有Cl2产生,可观察到的现象是__________________,写出反应方程式__________________.
(5)写出尾气吸收装置中进行的反应的化学方程式_______________________.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高二下学期期初化学试卷 题型:选择题
今有室温下四种溶液,有关叙述不正确的是( )
① | ② | ③ | ④ | |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A. ①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B. 分别加水稀释10倍,四种溶液的pH:①>②>④>③
C. 溶液中水的电离程度③>④
D. VaL④溶液与VbL②溶液混合后,若混合后溶液pH=4,则Va∶Vb=11∶9
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高二下学期期初化学试卷 题型:选择题
某无色透明的碱性溶液中,能大量共存的离子组是( )
A. Na+、H+、SO42﹣、HCO3﹣
B. Cu2+、K+、SO42﹣、NO3﹣
C. Na+、K+、Cl﹣、NO3﹣
D. Mg2+、K+、SO42﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市高三教学质量检测(一)理综化学试卷(解析版) 题型:填空题
向硫酸铜水溶液中逐滴加入氨水,先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,再向溶液中加入乙醇有深蓝色晶体(化学式为[Cu(NH3)4]SO4·H2O)析出。
(1)写出上述实验前两步反应的离子方程式__________,____________。
(2)铜元素基态原子的电子排布式为_________________,铜单质晶体中的原则堆积模型属于_________堆积(填堆积模型名称)。
(3)在上述深蓝色晶体所含的非金属元素中,电负性最大的是_________(填元素符号),第一电离能最大的是_________(填元素符号)。该晶体中的阴离子的立体构型是_________,阴离子的中心原子的杂化方式为_________。
(4)氨的沸点_________(填“高于”或“低于”)膦(PH2),原因是_____________。
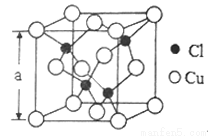
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式是______________。若该晶体的密度为pg·cm-3,以NA表示阿伏伽德罗常数,则该晶胞的边长为a=_____________nm。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省A10联盟高三下学期开年考试理综化学试卷(解析版) 题型:选择题
直接氨硼烷(NH3·BH3)电池可在常温下工作,装置如图。该电池的总反应为:NH3·BH3+3H2O=NH4BO2+4H2O。下列说法正确的是( )
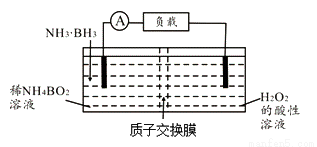
A. 左侧电极发生还原反应
B. 电池工作时,H+通过质子交换膜向负极移动
C. 正极的电极反应式为2H++2e-=H2↑
D. 消耗3.1g氨硼烷,理论上转移0.6mol电子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省石家庄市高一上学期期末考试化学试卷(解析版) 题型:选择题
下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、6 mol/L硫酸溶液、NaOH溶液。下列说法错误的是
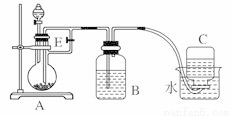
A. B中盛有一定量的NaOH溶液,A中应预先加入的试剂是铁屑
B. 实验开始时应先将活塞E关闭
C. 生成Fe(OH)2的操作为:关闭E,使A中溶液压入B瓶中
D. 取下装置B中的橡皮塞,使空气进入,有关反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com