
| A. | 由水电离出的c(H+)=1.0×10-2mol•L-1 | |
| B. | 醋酸的电离平衡常数Ka=c(CH3COO-)•c(H+) | |
| C. | 若将溶液的温度升高到100℃,c(OH-)减小 | |
| D. | 加水稀释后H+的物质的量增加 |
分析 A.酸或碱抑制水电离,酸溶液中水电离出的c(H+)=c(OH-);
B.电离平衡常数Ka=$\frac{c(C{H}_{3}CO{O}^{-}).c({H}^{+})}{c(C{H}_{3}COOH)}$;
C.升高温度,促进醋酸电离、水电离,且水的离子积常数增大;
D.加水稀释促进醋酸电离.
解答 解:A.酸或碱抑制水电离,该酸溶液中水电离出的c(H+)=c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-2}}$mol/L=1.0×10-10mol•L-1,故A错误;
B.电离平衡常数Ka=$\frac{c(C{H}_{3}CO{O}^{-}).c({H}^{+})}{c(C{H}_{3}COOH)}$,故B错误;
C.升高温度,促进醋酸电离、水电离,且水的离子积常数增大,溶液中c(OH-)增大,故C错误;
D.加水稀释促进醋酸电离,醋酸电离出的氢离子个数增多,则H+的物质的量增加,故D正确;
故选D.
点评 本题考查弱电解质的电离,为高频考点,明确弱电解质电离特点及离子积常数与温度关系是解本题关键,注意电离平衡常数表达式的书写,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z、W四种元素的简单氢化物中,Y的气态氢化物最稳定 | |
| B. | Y、Z、W四种元素的原子半径由大到小的顺序为:Y>Z>W | |
| C. | X、Z和W三种元素形成的简单离子的半径由大到小的顺序为:W>Z>X | |
| D. | Y、Z和W三种元素的最高价氧化物对应的水化物都是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)<c(H+) | B. | 溶液中c(OH-)>c(H+) | ||
| C. | c(OH-)=c(H+) | D. | c(OH-)>1×10-7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
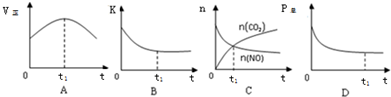
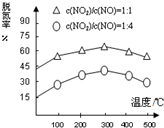

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
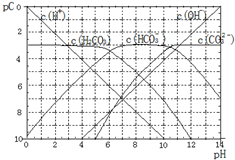
| A. | 某温度下,CO2饱和溶液的浓度是0.05mol•L-1,其中$\frac{1}{5}$的CO2转变为H2CO3,若此时溶液的pH约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度为0.1% | |
| B. | 25℃时,H2CO3一级电离平衡常数的数值Ka1=10-6 | |
| C. | 向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO${\;}_{3}^{2-}$)+c(OH-)+c(HCO${\;}_{3}^{-}$) | |
| D. | 25℃时,0.1mol/LNa2CO3中C(HCO${\;}_{3}^{-}$)比0.1mol/LH2CO3中C(HCO${\;}_{3}^{-}$)大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$Na2CO3(s) | B. | CuCl2$\stackrel{NaOH(aq)}{→}$Cu(OH)2$→_{△}^{乙醛}$Cu | ||
| C. | Al$\stackrel{NaOH(aq)}{→}$NaAlO2(aq)$\stackrel{△}{→}$NaAlO2(s) | D. | Al2O3(s)$\stackrel{HCl(aq)}{→}$AlCl3(aq)$\stackrel{通电}{→}$Al(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应发生的过程中,只放出能量 | |
| B. | 化学反应中的能量通常表现为热量的变化 | |
| C. | 锌与盐酸反应是吸热的过程 | |
| D. | 反应物的总能量高于生成物的总能量为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| O═O | H-H | H-O(g) | |
| 1 mol化学键断裂时需要吸收的能量/kJ | 496 | 436 | x |
| A. | 920 | B. | 557 | C. | 463 | D. | 188 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com