
分析 (1)反应有HCl剩余,溶液为NaCl、HCl、AlCl3混合溶液,同一溶液中离子浓度之比等于物质的量之比,令n(Al3+)、n(H+)、n(Cl-)分别为1mol、2mol、8mol,根据电荷守恒计算n(Na+),再根据原子守恒计算n(Al)、n(Na2O2),结合守恒,再根据m=nM计算;
(2)反应收集的气体为氢气、氧气,令氢气、氧气的物质的量分别为xmol、ymol,根据转移电子与气体体积列方程计算解答.
解答 解:(1)反应有HCl剩余,溶液为NaCl、HCl、AlCl3混合溶液,同一溶液中离子浓度之比等于物质的量之比,令n(Al3+)、n(H+)、n(Cl-)分别为1mol、2mol、8mol,根据电荷守恒,可知n(Na+)=n(Cl-)-n(H+)-3n(Al3+)=8mol-2mol-1mol×3=3mol,结合守恒可知,原混合物中n(Al)=n(Al3+)=1mol,n(O原子)=n(Na+)=3mol,故m(Al):(O元素)=1mol×27g/mol:3mol×16g/mol=9:16,
故答案为:9:16;
(2)反应收集的气体为氢气、氧气,令氢气、氧气的物质的量分别为xmol、ymol,根据转移电子与气体体积可得:$\left\{\begin{array}{l}{x+y=\frac{b}{22.4}}\\{2x+2y=a}\end{array}\right.$,整理的a:b=2:22.4,
故答案为:22.4.
点评 本题考查混合物计算,清楚发生的反应是解题关键,利用终态物质进行解答,注意守恒思想的应用,侧重对解题方法技巧与学生思维能力的考查,难度中等.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
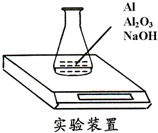 某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:
某种由Al与Al2O3粉末组成的混合物样品,利用如下图装置测定混合物中Al的质量分数(已知样品质量为2.58g、锥形瓶和过量NaOH溶液的总质量为185.72g),每隔相同时间读得电子天平的数据如下表:| 读数次数 | 质量(g) | |
| 锥形瓶 + NaOH溶液 + 试样 | 第1次 | 188.30 |
| 第2次 | 188.28 | |
| 第3次 | 188.25 | |
| 第4次 | 188.24 | |
| 第5次 | 188.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2+O2═2H2O△H=-142.9 kJ/mol | B. | 2H2(g)+O2(g)═2H2O(l)△H=-142.9 kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | D. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁作负极 | |
| B. | 正极材料可以是石墨 | |
| C. | 电解质可以是CuSO4溶液 | |
| D. | 0.2mol电子通过电解质移动向正极被0.2molCu2+得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A>B>C>D | B. | C>A>B>D | C. | A>C>D>B | D. | B>D>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
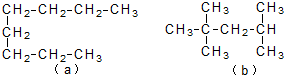
| A. | a和b都不能使酸性KMnO4溶液褪色 | |
| B. | a和b分子中的所有碳碳单键间的键角都相同 | |
| C. | a的沸点比b高 | |
| D. | b脱氢可以形成3种单烯烃分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com