
| A、NA个Fe(OH)3胶体粒子的质量为107g |
| B、1mol甲基的电子数目为9NA |
| C、标准状况下,2.24L Cl2溶于水中达到饱和,转移的电子数是0.1NA |
| D、2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0.2NA之间 |


科目:高中化学 来源: 题型:
| A、向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+═BaSO4↓+NH3?H2O+H2O |
| B、碘化钾与适量溴水反应:2I-+Br2═I2+2Br- |
| C、硫化钾的水解:S2-+2H2O?H2S+2OH- |
| D、向NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NH4HCO3溶于过量的浓KOH溶液中并加热:NH4++HCO3-+2OH-
| ||||
| B、Fe溶于足量稀硝酸:Fe+2H+﹦Fe2++H2↑ | ||||
| C、向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | ||||
| D、醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
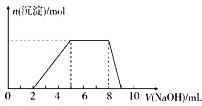 某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、[Al(OH)4]-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、[Al(OH)4]-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )| A、原溶液中一定含有的阳离子是H+、Mg2+、Al3+、NH4+ |
| B、反应最后形成的溶液中的溶质含AlCl3 |
| C、原溶液中Al3+与NH4+的物质的量之比为1:3 |
| D、原溶液中含有的阴离子是[Al(OH)4]-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将锌棒和石墨棒按如图所示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
将锌棒和石墨棒按如图所示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )| A、将电能转变为化学能 |
| B、电子由石墨棒流出 |
| C、锌为正极 |
| D、电池反应为:Zn+CuSO4═ZnSO4+Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com