
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气中点燃 | 产物分别为FeC13和CuC12 |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物分别为Fe2(SO4)3和CuSO4 |
| ④将铜片置于FeC13溶液中 | 铜片逐渐溶解 |
| ⑤将铁片和铜片插入盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
| A. | 2 种 | B. | 3 种 | C. | 4种 | D. | 5 种 |
分析 ①将铁片置于CuSO4溶液中,铁片上有亮红色物质析出,说明铁置换出了铜;
②氯气和金属反应时,氯气将金属氧化到最高价态;
③浓硫酸具有氧化性,可以将变价金属氧化到最高价;
④铜片置于FeCl3溶液中,会和三价铁发生反应生成亚铁离子和铜离子;
⑤在原电池中,负极金属的活泼性一般强于正极金属的活泼性.
解答 解:①铁置换出了铜,可以证明金属铁的活泼性强于金属铜,故①正确;
②氯气和金属反应时,氯气将金属铁和铜氧化到最高价态,不能证明金属的活泼性,故②错误;
③浓硫酸具有氧化性,可以将变价金属铁和铜氧化到最高价,不能证明金属的活泼性,故③错误;
④铜片置于FeCl3溶液中,会和三价铁发生反应生成亚铁离子和铜离子,只能证明还原性:Cu>Fe2+,氧化性是:Fe3+>Cu2+,不能证明铁的金属活动性比铜强,故④错误;
⑤将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接,形成的原电池中,负极金属Fe的活泼性强于正极金属Cu的活泼性,能证明铁的金属活动性比铜强,故⑤正确.
故选A.
点评 本题考查学生金属活泼性的判断方法,可以根据所学知识来回答,注意平时知识的积累,综合性较强,难度中等.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| 实验序号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| 1 | 锌 | 铜 | 菠萝 | 3 | 900 |
| 2 | 锌 | 铝 | 菠萝 | 3 | 650 |
| 3 | 锌 | 铝 | 苹果 | 3 | 450 |
| A. | 实验l 中锌为负极,电子由锌经导线流向铜 | |
| B. | 实验2 中铝为负极,铝失去电子,电流由锌经导线流向铝 | |
| C. | 实验3 中铝为负极,电极反应为Al-3e-═A13+ | |
| D. | 水果电池的电压只跟水果的品种有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 乙烷(乙烯) | 溴水 | 洗气 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 乙醇(水) | CaO | 蒸馏 |
| D | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
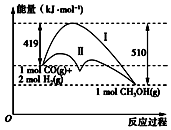 利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)=CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)=CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )| A. | 该反应物△H=+91 kJ•mol-1 | |
| B. | 加入催化剂,该反应的△H变小 | |
| C. | 曲线Ⅱ使用催化剂,降低了反应的活化能 | |
| D. | 如果该反应生成液态CH3OH,则△H增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3,用烧碱进行干燥 | |
| B. | 加热NH4HCO3,气体用五氧化二磷干燥 | |
| C. | 加热浓氨水,气体用碱石灰干燥 | |
| D. | 2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O,气体用无水氯化钙干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该装置能将电能转化为化学能 | B. | Zn为负极,Cu为正极 | ||
| C. | 电子由Cu电极经 流向Zn电极 流向Zn电极 | D. | 正极反应为 Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 126C、136C、146C三种核素互为同素异形体 | |
| B. | 溶液、胶体和悬浊液这三种分散系的本质区别是能否透过滤纸或半透膜 | |
| C. | 等质量的甲烷按a,b两种途径完全转化,途径a比途径b消耗更多的O2 途径a:CH4$→_{催化重整}^{H_{2}O}$CO+H2$→_{燃烧}^{O_{2}}$CO2+H2O;途径b:CH4$→_{燃烧}^{O_{2}}$CO2+H2O | |
| D. | 铝热反应实验说明:在一定条件下铝的还原性强于很多难熔金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
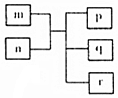 短周期主族元素X、Y、Z、W原子序数依次递增,Y原子最外层电子数为次外层电子数的二倍.m为元素Y的单质,n为元素Z的最高价氧化物的水化物,p、q、r分别为上述四种元素组成的二元化合物.下列说法正确的是( )
短周期主族元素X、Y、Z、W原子序数依次递增,Y原子最外层电子数为次外层电子数的二倍.m为元素Y的单质,n为元素Z的最高价氧化物的水化物,p、q、r分别为上述四种元素组成的二元化合物.下列说法正确的是( )| A. | 原子半径Y<Z<W | |
| B. | 简单气态氢化物的稳定性Y>Z>W | |
| C. | X与Z形成的化合物的水溶液一定为酸性溶液 | |
| D. | X、Z、W三种元素可以形成离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com