
硫铁矿烧渣的主要成分为Fe2O3、Fe3O4,以及少量SiO2、Al2O3等。由硫铁矿烧渣制备铁红(Fe2O3)的一种工艺流程如下:
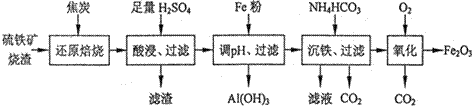
已知:还原焙烧时,大部分Fe2O3、Fe3O4转化为FeO。
几种离子开始沉淀和完全沉淀时的pH如下表所示:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
(1)“酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号) 。
(2)Fe粉除调pH外,另一个作用是 ;Fe粉调节溶液的pH为 。
(3)“沉淀、过滤”步骤中生成FeCO3的离子方程式为 ;
所得滤液的主要溶质是(填化学式) 。
(4)高温条件下,“氧化”步骤中发生反应的化学方程式为 。
【答案】(1)Fe2+、Fe3+、Al3+;(2)将溶液中Fe3+还原为Fe2+,便于与Al3+分离;5(4.7~7.6或其之间的任意数值);(3)Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;(NH4)2SO4;(4)FeCO3+O2 2Fe2O3+4CO2
2Fe2O3+4CO2
【解析】
试题分析:在硫铁矿烧渣中含有Fe2O3、Fe3O4,以及少量SiO2、Al2O3等,当加入酸时,Fe2O3、Fe3O4、Al2O3发生反应变为Fe2+、Fe3+、Al3+存在于溶液中;而SiO2不能溶解在酸中,被过滤除去;(2)由于Fe3+、Al3+形成沉淀时的溶液的pH接近,不容易分离,所以加入Fe粉除调pH外,另一个作用是将溶液中Fe3+还原为Fe2+,便于与Al3+分离;由于Al3+沉淀完全的溶液的pH=4.7,而Fe2+沉淀完全的溶液的pH=9.7,所以Fe粉调节溶液的pH为4.7~7.6或其之间的任意数值;(3)根据题意在“沉淀、过滤”步骤中生成FeCO3的离子方程式为Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;由于在过程中加入的是硫酸和NH4HCO3,所以所得滤液的主要溶质是(NH4)2SO4;(4)高温条件下,FeCO3 和O2 发生反应产生Fe2O3和CO2,根据电子守恒和元素的原子个数守恒可得该“氧化”步骤中发生反应的化学方程式为FeCO3+O2 2Fe2O3+4CO2。
2Fe2O3+4CO2。
考点:考查物质的性质、转化、反应条件的控制与选择、方程式的书写的知识。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个。下列叙述正确的是
A. Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应
B. 原子半径Z>W>Y>X
C. 气态氢化物的稳定性Z>W
D. X的气态氢化物与足量W单质在光照条件下反应生成物均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
含有下列各组离子的溶液中通入(或加入)过量的某种物质后仍能大量共存的是
A.H+、Ba2+、Fe3+、NO3-,通入SO2气体
B.Ca2+、Cl-、K+、H+,通入CO2气体
C.AlO2-、Na+、Br-、SO42-,通入CO2气体
D.HCO3-、Na+、I-、HS-,加入AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA 为阿伏加德罗常数的值。下列说法正确的是 ( )
A.标准状况下,2.24 L 水中所含的电子数为NA
B.常温常压下,16 g O3所含的电子数为8NA
C.0.1 mol Na2O2 晶体中所含的离子数为0.4NA
D.1 mol Fe在氧气中充分燃烧失去的电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用铂丝蘸取少量某无色溶液进行焰色反应 | 火焰呈黄色 | 该溶液一定是钠盐溶液 |
| B | 向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向溶液X中滴加稀盐酸 | 有气体产生 | 溶液X 中一定含有CO32- |
| D | 向含H2SO4的淀粉水解液中加入新制的Cu(OH)2,煮沸 | 没有砖红色沉淀 | 淀粉未水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到目的的是
A.用锌与稀硝酸制备H2 B.CaCO3中混有少量NaHCO3,可用加热的方法除去
C.可用蒸馏水来区分NO2和溴蒸气 D.用相互滴加的方法来鉴别AlCl3和氨水两瓶试剂
查看答案和解析>>
科目:高中化学 来源: 题型:
黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现为了测定某黄铜矿的纯度,某同学设计了如下实验,已知d中试剂能将所吸收的气体充分吸收:
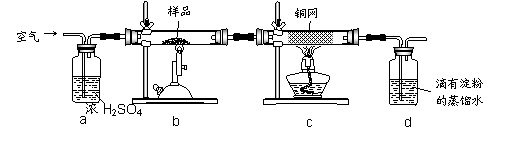 |
现称取研细的黄铜矿样品2.0g,在空气中煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的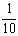 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.00mL,末读数如右图所示。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.00mL,末读数如右图所示。请回答下列问题:
(1)称量样品所用的仪器为 ,将样品研细后再反应,其目的是 。
(2)装置a的作用是 。
A、有利于空气中氧气充分反应 b、除去空气中的水蒸气
C、有利于气体混合 d、有利于观察空气流速
(3)b中发生的反应方程式为 。
 (4)滴定时,标准碘溶液所耗体积为 mL。
(4)滴定时,标准碘溶液所耗体积为 mL。
判断滴定已达终点的现象是______
。
(5)通过计算可知,该黄铜矿的纯度为 。
(6)若用右图装置替代上述实验装置d,同样
可以达到实验目的的是 。(填编号)
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温、恒压下,a mol A和b molB在一个容积可变的容器中发生反应:A(g)+2B(g)⇌2C(g),一段时间后达到平衡,生成n mol C.下列说法正确的( )
|
| A. | 物质A、B的转化率之比为l:2 |
|
| B. | 起始时刻和达到平衡后容器中的压强之比为(a+b):(a+b﹣) |
|
| C. | 当2v正(A)=v逆(B)时,反应一定达到平衡状态 |
|
| D. | 充入惰性气体,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
无色溶液可能由K2CO3、MgCl2、NaHCO3、BaCl2溶液中的一种或几种组成。向溶液中加入烧碱溶液出现白色沉淀,加入稀硫酸也出现白色沉淀并放出气体。据此分析,下列判断中正确的是( )
①肯定有BaCl2 ②肯定有MgCl2 ③肯定有NaHCO3
④肯定有Na2CO3或NaHCO3 ⑤肯定没有MgCl2
A.①②③ B.②④ C.①③ D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com