
(12分)低碳经济呼唤新能源和清洁环保能源。煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 850 |
平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
(1)该反应逆反应的化学平衡常数表达式为K = 。
(2)上述正反应方向是 反应(填“放热”或“吸热”)。
(3)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g)发生上述反应,CO和H2O(g)浓度变化如下图,则0~4 min的平均反应速率v(CO)= mol·L-1·min-1。

(4)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表。
①表中3 min~4 min之间反应处于 状态;C1数值 0.08 mol·L-1(填大于、小于或等于)。
②反应在4 min~5 min,平衡向逆方向移动,可能的原因是 (单选),表中5 min~6 min之间数值发生变化,可能的原因是 (单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
(5)若在500℃时进行,若CO、H2O的起始浓度均为0.020 mol·L-1,在该条件下,CO的最大转化率为: 。
(1)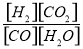 ;(2)放热;(3)0.03;(4)①平衡;大于;②D、A;(5)75%
;(2)放热;(3)0.03;(4)①平衡;大于;②D、A;(5)75%
【解析】
试题分析:(1)根据平衡常数的定义,该反应逆反应的化学平衡常数表达式为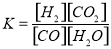 ;(2)升高温度,该反应平衡常数减小,所以正反应放热;(3)0~4 min的平均反应速率v(CO)
;(2)升高温度,该反应平衡常数减小,所以正反应放热;(3)0~4 min的平均反应速率v(CO)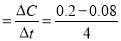 =0.03 mol·L-1·min-1;(4)①3 min~4 min时各物质的浓度均没变,所以处于平衡状态;850℃时,CO的平衡浓度为0.08 mol·L-1,升高温度,平衡左移,所以CO的平衡浓度增大,故C1数值大于0.08 mol·L-1;②4 min~5 min,CO、H2O的浓度都增大了0.036 mol·L-1,CO2的浓度减小0.036 mol·L-1,故改变的条件为增加氢气浓度;5 min~6 min CO浓度减小,H2O浓度增大,所以改变的条件为增加水蒸气;(5)500℃时K=9,设消耗的CO的浓度为x,则CO平衡浓度为(0.020—x) mol·L-1,H2O的平衡浓度为(0.020—x) mol·L-1,CO2的平衡浓度x、H2的平衡浓度x;
=0.03 mol·L-1·min-1;(4)①3 min~4 min时各物质的浓度均没变,所以处于平衡状态;850℃时,CO的平衡浓度为0.08 mol·L-1,升高温度,平衡左移,所以CO的平衡浓度增大,故C1数值大于0.08 mol·L-1;②4 min~5 min,CO、H2O的浓度都增大了0.036 mol·L-1,CO2的浓度减小0.036 mol·L-1,故改变的条件为增加氢气浓度;5 min~6 min CO浓度减小,H2O浓度增大,所以改变的条件为增加水蒸气;(5)500℃时K=9,设消耗的CO的浓度为x,则CO平衡浓度为(0.020—x) mol·L-1,H2O的平衡浓度为(0.020—x) mol·L-1,CO2的平衡浓度x、H2的平衡浓度x; ,x=0.015 mol·L-1,所以CO的最大转化率为
,x=0.015 mol·L-1,所以CO的最大转化率为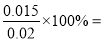 75%。
75%。
考点:本题考查化学反应速率、平衡常数、平衡转化率。


科目:高中化学 来源:2014秋福建省高二上学期期中化学(文)试卷(解析版) 题型:实验题
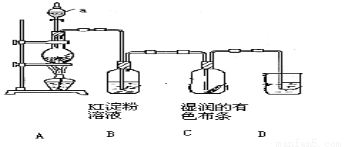
(18分)某化学研究性学习小组设计制取氯气及探究其性质的方案,并按下图所示装置完成实验。(A中发生反应的化学方程式为:MnO2 + 4HCl(浓) ==== MnCl2 + Cl2↑ + 2H2O)
【实验探究】
(1)装置A中,仪器a的名称是 。
(2)装置B中无色溶液将变为 色,该反应的化学方程式是 。
(3)装置C中湿润的有色布条 (填“褪色”或“不褪色”),其原因是氯气与水反应生成了 (填化学式)
(4)为了吸收多余的氯气,防止造成空气污染,装置D中应盛放 ____溶液(填“NaOH”或“H2SO4”)
(5)用8.7gMnO2与足量浓盐酸反应,理论上可以生成标准状况下的Cl2 _______L。
【知识拓展】
(6)某同学查阅资料得知:高锰酸钾与浓盐酸在常温下也可以生成氯气(反应的化学方程式为:
2KMnO4 + 16HCl(浓) ==== 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O),该反应的氧化剂是 (填“KMnO4”或“HCl”)
【知识应用】
(7)洪灾过后,饮用水的消毒杀菌是抑制大规模传染疾病爆发的重要措施之一。请你列举一例对饮用水进行消毒杀菌的合理方法:______________________________________________________________________
查看答案和解析>>
科目:高中化学 来源:2014秋湖北省武汉市高二上学期期中联考化学试卷(解析版) 题型:选择题
化学反应N2+3H2 2NH3的能量变化如图所示,该反应的热化学方程式是
2NH3的能量变化如图所示,该反应的热化学方程式是
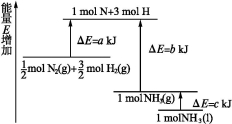
A.N2(g)+H2(g) = NH3(l) ΔH=+(b+c-a) kJ·mol-1
B.N2(g)+3H2(g) = 2NH3(g) ΔH=+2(b-a) kJ·mol-1
C.N2(g)+3H2(g) = 2NH3(l) ΔH=-2(b+c-a) kJ·mol-1
D.N2(g)+H2(g) = NH3(g) ΔH=+(a+b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014秋湖北省武汉市高一上学期期中联考化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.化学实验中不能把鼻孔凑到容器口去闻药品的气味,不得尝任何药品的味道。
B.过滤实验中若发现滤液浑浊,采取的措施是重新过滤。
C.用CCl4萃取碘水中的碘后,若再从CCl4中提取碘,应采用的方法是蒸馏而不是蒸发。
D.若夜晚发现家中天然气泄漏,不能开灯,应立即打开抽油烟机。
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
下图是可逆反应A(g)+2B(g) 2C(g)+3D(g),(正反应△H>0)的化学反应速率与化学平衡随外界条件改变而变化的关系图,下列条件的改变与图中情况相符的是:
2C(g)+3D(g),(正反应△H>0)的化学反应速率与化学平衡随外界条件改变而变化的关系图,下列条件的改变与图中情况相符的是:
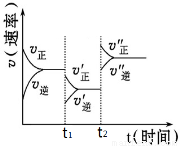
A.t1时,减小了A或B的物质的量的浓度
B.t2时,升高了温度
C.t2时,增大了压强
D.t1时,加了催化剂
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
将炭粉和铁粉均匀混合,撒入内壁分别用氯化钠溶液和稀醋酸溶液润湿过的具支试管中,并按下图装置好仪器,观察下图,示意正确的是

查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高一上学期期中考试化学试卷(解析版) 题型:填空题
(2分)在KCl、ZnCl2、ZnSO4三种盐配成的混合溶液中,已知K+为0.1mol、Zn2+为0.25mol,Cl-为0.2mol,则SO42-为 mol.
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:选择题
下列关于催化剂的说法正确的是
A.使用催化剂可以增大正反应速率,减小逆反应速率
B.使用催化剂可以使化学平衡正向移动
C.使用催化剂可以降低反应的活化能
D.使用催化剂可以改变反应的平衡常数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com