
已知NH4CuSO3与足量的10mol/L硫酸液混合微热,产生下列现象:
①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色
据此判断下列说法正确的是
A.反应中硫酸作氧化剂 B.NH4CuSO3中硫元素被氧化
C.刺激性气味的气体是氨气 D.1molNH4CuSO3完全反应转移0.5mol电子
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表; J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的元素。
J |
|
|
|
|
|
| R |
|
|
下列说法错误的是( )
A .J的单质一定能导电
B.J、R形成的化合物JR2中J与R原子间是极性共价键
C.R、T两元素的气态氢化物中,T的气态氢化物更稳定
D.四种元素中T的最高价氧化物的水化物酸性最强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上月考四化学卷(解析版) 题型:选择题
常温下,用 0.1000mol•L-1NaOH溶液滴定 20.00mL 0.1000mol•L-1CH3COOH溶液所得滴定曲线如图.下列说法不正确的是
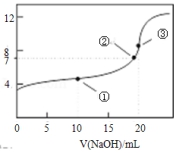
A.点①所示溶液中:c(CH3COO-)+c(CH3COOH)=2c(Na+)
B.点②所示溶液中:c(Na+)=c(CH3COO-)
C.点③所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
D.滴定过程中可能出现:c(CH3COOH)>c(H+)>c(CH3COO-)>c(Na+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高一上期中化学卷(解析版) 题型:选择题
关于一些重要 的化学概念有下列说法:
的化学概念有下列说法:
①Fe(OH)3胶体和CuSO4溶液都是混合物;
②BaSO4是一种难溶于水的强电解质;
③醋酸、纯碱、小苏打分别属于酸、碱、盐;
④根据纯净物的元素组成,将纯净物分为单质和化合物;
⑤金属氧化物都是碱性氧化物;
⑥某元素从化合态变为游离态时,该元素一定被还原;
其中正确的是 ( )
A.①②⑤⑥ B.①②④ C.②③④ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上11月月考化学卷(解析版) 题型:填空题
高锰酸钾在不同的条件下发生的反应如下:
MnO4-+5e-+8H+═Mn2++4H2O ①
MnO4-+3e-+2H2O═MnO2↓+4OH- ②
MnO4-+e-═MnO42-(溶液呈绿色) ③
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的_________影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为_________→_________。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的是_________(填字母)
A.氧化性:PbO2>KMnO4 B.Mn2+被还原成MnO4- c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量比为3:2。
完成下列化学方程式:
①_______KMnO4+_______ K2S+_______→ _______K2MnO4+ ______ K2SO4+_______ S↓+ ______
②若生成6.4g单质硫,反应过程中转移的电子的物质的量为 _________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上11月月考化学卷(解析版) 题型:选择题
在甲、乙两烧杯溶液中,共含有大量的Cu2+、Na+、H+、SO42-、CO32-、OH-等6种离子.已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是
A.Cu2+、H+、SO42- B.Na+、OH-、CO32-
C.CO32-、OH-、SO42- D.Na+、H+、SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上11月月考化学卷(解析版) 题型:选择题
在反应H2S+H2SO4(浓)=S↓+SO2↑+2H2O中,若有32g硫生成则转移电子为
A.6mol B.2mol C.3mol D.4mol
查看答案和解析>>
科目:高中化学 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:简答题
人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
(1)工业上常用高浓度的K2CO3 溶液吸收CO2,得溶液X,再利用电解法使K2CO3  溶液再生,其装置示意图如下:
溶液再生,其装置示意图如下:
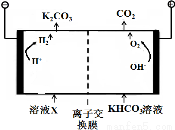
①在阳极区发生的反应包括 和H++HCO3- H2O+CO2↑。
H2O+CO2↑。
②简述CO32-在阴极区再生的原理 。
(2)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25 ℃,101 KPa下:
H2(g)+ 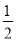 O2(g)
O2(g) H2O(g)ΔH1=-242kJ·mol-1
H2O(g)ΔH1=-242kJ·mol-1
CH3OH(g)+(3/2) O2(g) CO2(g)+2H2O(g)ΔH2=-676kJ·mo
CO2(g)+2H2O(g)ΔH2=-676kJ·mo l-1
l-1
①写出CO2和H2生成气态甲醇等产物的热化学方程式 。
②下面表示合成甲醇的反应的能量变化示意图,其中正确的是 (填字母序号)。
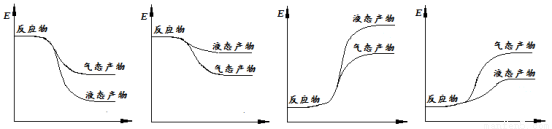
A B C D
(3)微 生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
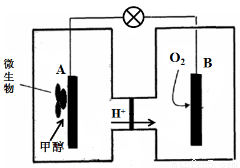
①该电池外电路电子的流动方向为 (填写“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津静海一中等六校高一上期中化学卷(解析版) 题型:选择题
已知Fe3O4可表示成(FeO·Fe2O3),水热法制备Fe3O4纳米颗粒的总反应为: 3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O,下列说法正确的是( )
A.O2和S2O32-是氧化剂,Fe2+是还原剂
B.每生成1mol Fe3O4,则转移电子数为2mol
C.参加反应的氧化剂与还原剂的物质的量之比为1:1
D.若有2mol Fe2+被氧化,则被Fe2+还原的O2为0.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com