
下列实验操作可以达到实验目的是( )
| 实验目的 | 实验操作 | |
| A. | 验证乙炔能被酸性高锰酸钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| B. | 检验淀粉水解产物的还原性 | 取少量淀粉溶液,与稀硫酸共热后再加入银氨溶液,水浴加热,观察是否出现银镜 |
| C. | 除去乙酸乙酯中混有的少量乙酸 | 加入足量饱和Na2CO3溶液,振荡,静置,分液,取出上层液体 |
| D. | 检验溴乙烷中的溴元素 | 取少量溴乙烷,与氢氧化钠溶液共热后加入硝酸银溶液,观察是否出现白色沉淀 |
|
| A. | A | B. | B | C. | C | D. | D |
考点:
化学实验方案的评价.
专题:
实验评价题.
分析:
A.电石不纯,与水反应生成乙炔的同时也生成硫化氢、磷化氢等;
B.银镜反应应在碱性条件下进行;
C.乙酸乙酯不溶液饱和碳酸钠溶液,而乙酸可与碳酸钠反应;
D.应先酸化后再检验.
解答:
解:A.电石不纯,与水反应生成乙炔的同时也生成硫化氢、磷化氢等,都可与高锰酸钾溶液反应,应先除杂,故A错误;
B.银镜反应应在碱性条件下进行,题中没有加入碱调节溶液pH,故B错误;
C.乙酸和碳酸钠反应生成可溶性的乙酸钠,乙酸乙酯和碳酸钠不反应且乙酸乙酯不溶于水,然后采用分液的方法分离,所以能实现实验目的,故C正确;
D.溴乙烷在碱性条件下水解生成溴离子,应先酸化后再检验,否则生成AgOH沉淀而影响实验结果,故D错误.
故选C.
点评:
本题考查了实验方案的评价,为高频考点,侧重于学生的分析能力和实验能力的考查,涉及物质的分离和提纯、物质的检验等知识点,根据物质的性质确定除杂剂,再结合物质反应条件来分析解答,易错选项是AD,注意:银镜反应及醛、新制Cu(OH)2悬浊液反应都必须在碱性条件下,为易错点.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
室温下,甲溶液中水电离出的H+浓度为10﹣12 mol•L﹣1,乙溶液中水电离出的H+浓度为10﹣2 mol•L﹣1,下列说法中正确的是( )
|
| A. | 甲、乙两溶液的pH不可能相同 |
|
| B. | 甲、乙两种溶液中加入Al粉都会产生H2 |
|
| C. | HCO3﹣ 不可能在甲、乙两溶液中大量共存 |
|
| D. | 甲不可能是盐溶液,乙不可能是酸或碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)⇌Si(g)+4HCl(g);△H=+Q kJ•mol﹣1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
|
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 |
|
| B. | 若反应开始时SiCl4为1mol,则达平衡时,吸收热量为Q kJ |
|
| C. | 反应至4min时,若HCl浓度为0.24 mol/L,则H2的反应速率为0.03 mol/(L•min) |
|
| D. | 当反应吸收热量为0.025Q kJ时,生成的HCl通入100mL 1mol•L﹣1的NaOH溶液恰好反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是()
选项 X Y Z 箭头上所标数字的反应条件
A CaO Ca(OH)2 CaCO3 ①常温遇水
B AlCl3 NaAlO2 Al(OH)3 ②通入CO2
C Na2CO3 NaOH NaHCO3 ④过量Ca(OH)2溶液
D Cl2 Ca(ClO)2 HClO ③加浓盐酸
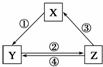
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
将镁、铝的混合物共0.2mol,溶于200mL 4mol•L﹣1的盐酸溶液中,然后再滴加2mol•L﹣1的NaOH溶液.请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示.当V1=160mL时,则金属粉末中n (Al)= mol
(2)0~V1段发生的反应的离子方程式为 ;
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)= mL;
(4)若镁、铝的混合物仍为0.2mol,其中镁粉的物质的量分数为a,改用200mL 4mol•L﹣1的硫酸溶解此混合物后,再加入840mL 2mol•L﹣1的NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为 .

查看答案和解析>>
科目:高中化学 来源: 题型:
1﹣丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是( )
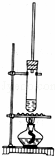
|
| A. | 不能用水浴加热 |
|
| B. | 长玻璃管有冷凝回流作用 |
|
| C. | 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
|
| D. | 加入过量乙酸可以提高1﹣丁醇的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟基(﹣OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
已知298K时,Mg(OH)2的溶度积常数KSP=5.6×10-12,取适量的MgCl2溶液,
加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是
A.所得溶液中的c (H+)=10-13mol/L
B.所得溶液中由水电离产生的c (OH-)=10-13 mol/L
C.所加的烧碱溶液的pH=13.0
D.所得溶液中的c (Mg2+)=5.6×10-10 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
20℃时,将10mL 0.1mol/L Na2S2O3溶液和10mL 0.1mol/L的H2SO4溶液混合,3min后溶液中明显出现浑浊.已知温度每升高10℃,化学反应速度增大到原来的3倍,那么40℃时,同样的反应要同样看到浑浊,需要的时间是( )
|
| A. | 40s | B. | 15s | C. | 30s | D. | 20s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com