
ClO2是一种杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 = 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是
A.KClO3在反应中得到电子
B.ClO2被氧化
C.H2C2O4在反应中被还原
D.1 mol KClO3参加反应有2 mol电子转移
科目:高中化学 来源:2014-2015山东省聊城市高一上学期第三次月考化学试卷(解析版) 题型:选择题
在MgCl2和AlCl3的混合溶液中加入过量的氨水,下图中能正确表示加入氨水的量(x)与生成沉淀的量(y)的关系的是

查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末化学试卷(解析版) 题型:选择题
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠。已知该电池放电时的电极反应式为:正极:FePO4+Li++e-=LiFePO4,负极:Li-e-=Li+。下列说法中正确的是
A.充电时的总反应为FePO4+Li=LiFePO4
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
查看答案和解析>>
科目:高中化学 来源:2014-2015辽宁省大连市高二上学期期末化学试卷(解析版) 题型:选择题
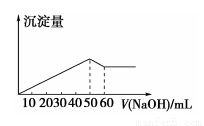
恒容密闭容器中进行的可逆反应2NO2 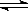 2NO +O2,可作为达到平衡状态的标志是
2NO +O2,可作为达到平衡状态的标志是
①单位时间内生成a mo1 O2的同时生成2a mol NO2 ;
②单位时间内生成a mol O2的同时生成2a molNO;
③混合气体的颜色不再改变;
④混合气体的密度不再改变的状态;
⑤混合气体的平均相对分子质量不再改变的状态。
A.①②③④⑤ B.②④⑤ C.①③④ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省等三校高一12月联考化学试卷(解析版) 题型:选择题
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合溶液中Al2(SO4)3与MgSO4的物质的量浓度之比为
A.6∶1 B.3∶1 C.2∶1 D.1∶2
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省等三校高一12月联考化学试卷(解析版) 题型:选择题
下列离子方程式中,正确的是
A.氢氧化钠溶液中通入过量CO2: CO2+2OH-= CO32-+H2O
B.金属铜与稀盐酸反应:Cu+2H+ = Cu2++H2↑
C.Ca(OH)2溶液与Na2CO3溶液反应:Ca2++CO32- = CaCO3↓
D.氯化铝与过量氨水反应:Al3++4OH-= AlO2-+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省等三校高一12月联考化学试卷(解析版) 题型:选择题
高一学生小强的化学笔记中有如下内容:
①纯净物按照组成可以分为单质和化合物
②单质又可分为金属和非金属
③无机化合物主要包括:酸、碱、盐和氧化物
④按照分散剂粒子直径大小可将分散系分为溶液、浊液和胶体
⑤水溶液能导电的化合物就是电解质
⑥按照树状分类法可将化学反应分为:氧化还原反应和离子反应
⑦氧化还原反应的特征是化合价升降
你认为他的笔记中有几处错误
A.三处 B.四处 C.五处 D.六处
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高一上学期期中考试化学试卷(解析版) 题型:选择题
同温同压下,等质量的下列气体所占有的体积最大的是
A.O2 B.CH4 C.CO2 D.SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高二上学期第三次月考化学试卷(解析版) 题型:填空题
(12分)下图是一个化学过程的示意图。
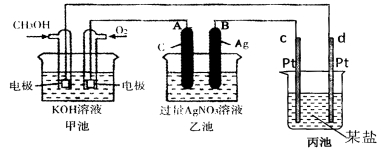
(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是 (填序号)
A.MgSO4 B.CuSO4 C.NaCL D.AgNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com