
| A. | 15 | B. | 16 | C. | 17 | D. | 18 |
分析 n(NaOH)=$\frac{3.00}{40g/mol}$=0.075mol,油脂与氢氧化钠按物质的量1:3反应,可知油脂的物质的量为0.025mol,结合M=$\frac{m}{n}$及分子构成计算.
解答 解:n(NaOH)=$\frac{3.00}{40g/mol}$=0.075mol,油脂与氢氧化钠按物质的量1:3反应,可知油脂的物质的量为$\frac{0.075mol}{3}$=0.025mol,
该油脂的摩尔质量为$\frac{22.25g}{0.025mol}$=890g/mol,故其相对分子质量为890,
饱和脂肪酸的通式为CxH2x+1COOCH2-CH(CxH2x+1COO)-CH2CxH2x+1COO,相对分子质量为42x+175,
则42x+175=890,
解得x=17.02.可知脂肪酸为C16H33COOH,
故选C.
点评 本题考查有机反应的计算,为高频考点,把握皂化反应中物质的量关系、油脂的组成等为解答的关键,侧重分析与计算能力的考查,注意油脂为高级脂肪酸甘油酯,题目难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②⑧ | C. | ③⑤ | D. | ⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀pH | 1,9 | 7.0 | 6,7 |
| 沉淀完全pH | $\frac{3}{4}$ | 9.0 | 10.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将氯化铝溶液滴入浓氢氧化钠溶液中,立刻产生大量白色沉淀 | |
| B. | Al2O3和MgO均可与NaOH溶液反应 | |
| C. | A1Cl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 常温下,Al(OH)3既能与NaOH溶液反应又能与稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
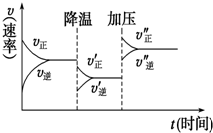 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况.由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况.由此可推断( )| A. | 正反应是放热反应 | B. | D可能是气体 | ||
| C. | 逆反应是放热反应 | D. | A、B、C、D均为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 组成上一个或若干个CH2原子团,且符合同一通式的有机物互称为同系物 | |
| B. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| C. | 苯的邻位二元取代物只有一种说明苯环中不存在单双键交替 | |
| D. | CH3-CH3+Cl2→CH2ClCH2Cl的反应类型为加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com