
【题目】常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如图所示。下列说法正确的是

A. 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
B. 当V=5时:c(CO32—)+c(HCO3-)+c(H2CO3)=c(Cl-)
C. 当V=10时:c(Na+)>c(HCO3-)>c(CO32—)>c(H2CO3)
D. 当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-)
【答案】D
【解析】A.当V=0时为碳酸钠溶液,根据电荷守恒有:c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-),根据物料守恒有:c(Na+)=2c(HCO3-)+2c(H2CO3)+2c(CO32-),联立可得:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-),故A错误;B.当V=5时,得到等浓度的NaHCO3、NaCl、Na2CO3混合溶液,根据物料守恒,c(CO32—)+c(HCO3-)+c(H2CO3)=2c(Cl-),故B错误;C.当V=10时,反应恰好生成等浓度的NaHCO3、NaCl的混合溶液,碳酸氢钠的水解程度大于电离程度,溶液显碱性,则c(H2CO3)>c(CO32—),故C错误;D.v=a时,溶液的pH=7,溶液为中性,则c(H+)=c(OH-),根据电荷守恒可得:c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(Cl-)+c(HCO3-),联立可得c(Na+)=2c(CO32-)+c(HCO3-)+c(Cl-),所以c(Na+)>c(Cl-)>c(H+)=c(OH-),故D正确;故选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在无色透明的碱性溶液中能大量共存的离子组是
A.Fe3+、Na+、Cl-、HCO3-B.K+、Na+、NO3-、CO32-
C.Mg 2+、H+、NO3-、SO42-D.K+、MnO4-、Na+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.C2H6和C4H10一定是同系物
B.C2H4和C4H8一定都能使溴水褪色
C.C3H6不只表示一种物质
D.单烯烃各同系物中碳的质量分数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对药物的认识和使用的说法,正确的是( )
A.麻黄碱属于非处方药
B.感冒时服用适量阿司匹林
C.冰毒和海洛因不是毒品
D.大部分药物都没有毒副作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
I.污染物SO2、NO2经O2预处理后用CaSO3悬浊液吸收,可减少尾气中SO2、NOx的含量。
T℃时,O2氧化烟气中SO2、NOx的主要反应的热化学方程式为:

(1)T℃时,反应3NO(g)+O3(g) ![]() 3NO2(g)的△H=_______________kJ.mol-1。
3NO2(g)的△H=_______________kJ.mol-1。
(2)T℃时,将0.6molNO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图1所示。
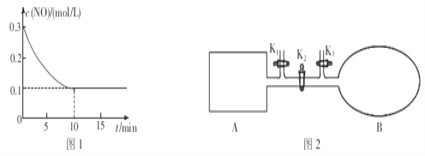
①T℃时,反应3NO(g)+O3(g)![]() 3NO2(g)的平衡常数K=______________。
3NO2(g)的平衡常数K=______________。
②不能说明反应达到平衡状态的是______________。
A.气体颜色不再改变 B.气体的平均摩尔质量不再改变
C.气体的密度不再改变 D.单位时间内生成O3和NO2物质的量之比为1:3
II.NO2的二聚体N2O4是火箭中常用氧化剂。完成下列问题:
(3)如图2所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊。关闭K2,将各1 molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL(忽略导管中的气体体积)。
①若容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)=________________。
②若打开K2,平衡后B容器的体积缩至0.4aL,则打开K2之前,气球B体积为__________L。
③若平衡后在A容器中再充入0.5molN2O4,则重新到达平衡后,平衡混合气中NO2的体积分数______________(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,密闭容器中发生反应aX(g) ![]() bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是( )
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是( )
A.可逆反应的化学方程式的化学计量数:a>b+c
B.压缩容器的容积时,v(正)增大,v(逆)减小
C.达到新平衡时,物质X的转化率减小
D.达到新平衡时,混合物中Z的质量分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中的可逆反应:mX(g)+nY(s) ![]() pZ(g) ΔH<0,达到平衡后,改变条件,下列表述不正确的是
pZ(g) ΔH<0,达到平衡后,改变条件,下列表述不正确的是
A.增大压强,化学平衡不一定发生移动
B.通入氦气,化学平衡不一定发生移动
C.增加X或Y的物质的量,化学平衡一定发生移动
D.其他条件不变,升高温度,化学平衡一定发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同的载体(钛片、铝片、陶瓷)表面制备TiO2薄膜,探究不同载体下TiO2薄膜光催化使甲基橙脱色的效果,每光照20 min取一次样,实验结果如图所示。下列说法正确的是( )
A.不同载体,无论何种温度一定是钛片载体的光催化活性最好
B.约在520 ℃时,钛片载体的光催化活性最好
C.无论何种载体,催化活性总是随温度的升高而升高
D.不同载体,TiO2薄膜的光催化活性相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com