
 (4)沉淀:生成沉淀碱式碳酸钴[(CoCO3)2•3Co(OH)2],沉淀需洗涤,洗涤的操作是向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次.
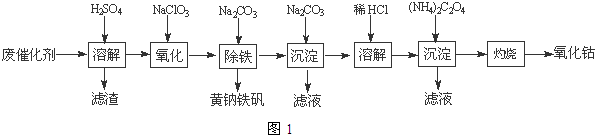
(4)沉淀:生成沉淀碱式碳酸钴[(CoCO3)2•3Co(OH)2],沉淀需洗涤,洗涤的操作是向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次.分析 钴废催化剂加入稀硫酸,发生Co+H2SO4=CoSO4+H2↑,Fe+H2SO4=FeSO4+H2↑,过滤滤渣是不溶的二氧化硅,而滤液是硫酸钴、硫酸亚铁与过量的硫酸的混合溶液,向滤液中加氯酸钠将亚铁离子氧化成铁离子,然后加入碳酸钠得到黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,继续向滤液中加入碳酸钠,得到碱式碳酸钴[(CoCO3)2•3Co(OH)2],然后用盐酸溶解碱式碳酸钴[(CoCO3)2•3Co(OH)2],再向所到溶液中加入草酸铵,得到溶解度极小的草酸钴,最后燃烧生成氧化钴,
(1)洗液与滤液合并,提高洗涤和滤液中钴的利用率,滤渣应该是原料中不溶于稀硫酸的成分;
(2)亚铁离子被氯酸根离子氧化成铁离子,根据得失电子守恒分析解答;根据3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色沉淀);4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3↓(蓝色沉淀),如果亚铁离子部分氧化,滴加无色的硫氰化钾生成蓝色沉淀,可向氧化后的溶液中滴入硫氰化钾,观察是否有蓝色沉淀生成;
(3)生成硫酸铁与碳酸钠发生双水解得到黄钠铁矾,书写化学方程式;
(4)沉淀洗涤的方法是向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次;
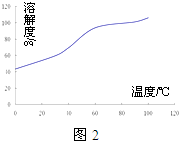
(5)CoCl2的溶解度曲线可知,随温度的升高,CoCl2的溶解度增大,所以趁热过滤,防止温度降低氯化钴析出;
(6)CoC2O4的质量为1.470g,其我知道可为0.01mol,Co元素质量为0.59g,钴氧化物质量为0.83g,氧化物中氧元素质量为0.83g-0.59g=0.24g,则氧化物中Co原子与O原子物质的量之比为0.01mol:$\frac{0.24}{16}$≈2:3,据此可确定该氧化物的化学式.
解答 解:钴废催化剂加入稀硫酸,发生Co+H2SO4=CoSO4+H2↑,Fe+H2SO4=FeSO4+H2↑,过滤滤渣是不溶的二氧化硅,而滤液是硫酸钴、硫酸亚铁与过量的硫酸的混合溶液,向滤液中加氯酸钠将亚铁离子氧化成铁离子,然后加入碳酸钠得到黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,继续向滤液中加入碳酸钠,得到碱式碳酸钴[(CoCO3)2•3Co(OH)2],然后用盐酸溶解碱式碳酸钴[(CoCO3)2•3Co(OH)2],再向所到溶液中加入草酸铵,得到溶解度极小的草酸钴,最后燃烧生成氧化钴,
(1)洗液与滤液合并,可提高洗涤和滤液中钴的利用率;所得滤渣为二氧化硅,化学式为:SiO2,
故答案为:提高钴等元素的利用率;SiO2;
(2)亚铁离子被氯酸根离子氧化成铁离子,1molr的亚铁离子失去1mol的电子,而1mol的氯酸根离子得到6mol的电子,根据电子得失守恒,可知离子方程式为:6Fe2++6H++ClO3-$\frac{\underline{\;\;△\;\;}}{\;}$6Fe3++Cl-+3H2O,取氧化后的溶液少许于试管中,滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,则Fe2+已全部被氧化,
故答案为:6Fe2++6H++ClO3-$\frac{\underline{\;\;△\;\;}}{\;}$6Fe3++Cl-+3H2O;取氧化后的溶液少许于试管中,滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,则Fe2+已全部被氧化;
(3)生成硫酸铁与碳酸钠发生双水解得到黄钠铁矾,化学反应方程式为:3Fe2(SO4)3+6H2O+6 Na2CO3=Na2Fe6(SO4)4(OH)12↓+5 Na2SO4+6CO2↑,
故答案为:3Fe2(SO4)3+6H2O+6 Na2CO3=Na2Fe6(SO4)4(OH)12↓+5 Na2SO4+6CO2↑;
(4)沉淀洗涤的方法是:向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次,
故答案为:向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次;
(5)CoCl2的溶解度曲线可知,随温度的升高,CoCl2的溶解度增大,所以趁热过滤,防止温度降低氯化钴析出,
故答案为:防止因温度降低,CoCl2晶体析出;
(6)CoC2O4的质量为1.470g,其我知道可为0.01mol,Co元素质量为0.59g,钴氧化物质量为0.83g,氧化物中氧元素质量为:0.83g-0.59g=0.24g,则氧化物中Co原子与O原子物质的量之比为0.01mol:$\frac{0.24}{16}$≈2:3,故Co氧化物为Co2O3,
故答案为:Co2O3.
点评 本题通过制取氧化钴,考查了物质制备方案的设计,题目难度中等,根据制备流程明确实验原理为解答关键,注意掌握常见化学实验基本操作方法,能够正确书写反应的化学方程式、离子方程式,试题知识点较多、综合性较强,充分考查了学生的分析能力及化学实验能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 只要摄入反式脂肪酸,就一定会患上心血管疾病 | |
| B. | 氢化是一种把液态植物油转化成固态或半固态脂肪的化学工艺 | |
| C. | 奶油、代可可脂巧克力、乳饮料、奶茶、蛋黄派等零食都可能含有反式脂肪酸 | |
| D. | 食品标签里的氢化植物油、植脂末、起酥油、代可可脂等都可能是反式脂肪酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2+H2O?H2SO3 | B. | SO2+2NaOH?Na2SO3+H20 | ||
| C. | 2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3 | D. | SO2+CaO═CaSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
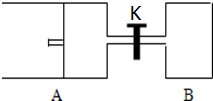 如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0达到平衡时,V(A)=1.2aL.试回答:
如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0达到平衡时,V(A)=1.2aL.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
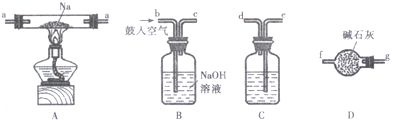
| 猜想 | 实验设计 | 现象与结论 |
| 剩余气体为H2(或O2). | 将b中剩余气体通过灼热的氧化铜 (或将b中剩余气体通过灼热的铜网). | 若看到黑色固体变红(或红色固体变黑), 证明此猜想正确,反之则不正确. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
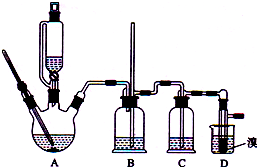 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
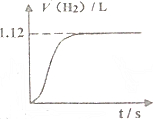 常温下在1LpH=3的HA溶液中加入过量铁粉,产生氢气的体积随时间变化的曲线如图所示(氢气体积已折算成标准状况下的体积)
常温下在1LpH=3的HA溶液中加入过量铁粉,产生氢气的体积随时间变化的曲线如图所示(氢气体积已折算成标准状况下的体积)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
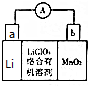 锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用,因此锂元素被誉为“能源元素”.请回答下列问题:
锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用,因此锂元素被誉为“能源元素”.请回答下列问题: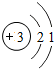 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com