
【题目】乳酸亚铁晶体{CH3CH(OH)COO]2Fe·3H2O}是一种很好的食品铁强化剂,易溶于水,广泛应用于乳制品、营养液等,吸收效果比无机铁好,可由乳酸与FeCO3反应制得:2CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O+CO2↑
Ⅰ.制备碳酸亚铁(FeCO3):装置如图所示。
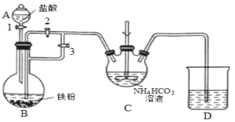
(1)仪器C的名称是______。
(2)清洗仪器,检查装置气密性,A中加入 盐酸,B中加入铁粉,C中加入NH4HCO3溶液。为顺利达成实验目的,上述装置中活塞的打开和关闭顺序为:关闭活塞_____,打开活塞_____,装置B中可观察到的现象是_____,当加入足量盐酸后,关闭活塞1,反应一段时间后,关闭活塞_____,打开活塞_____。C中发生的反应的离子方程式为_____。
Ⅱ. 制备乳酸亚铁晶体:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸。
(3)加入少量铁粉的作用是_____。从所得溶液中获得乳酸亚铁晶体所需的实验操作是隔绝空气低温蒸发,冷却结晶、过滤、洗涤、干燥。
Ⅲ.乳酸亚铁晶体纯度的测量:
(4)若用KMnO4滴定法测定样品中Fe2+的量进而计算纯度时,发现结果总是大于100%,其原因可能是_____。
(5)经查阅文献后,改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取5.76g样品,溶解后进行必要处理,用容量瓶配制成250mL溶液,每次取25.00 mL,用0.100mol/LCe(SO4)2标准溶液滴定至终点,记录数据如表所示。
滴定次数 | 0.100mol/LCe(SO4)2标准溶液/mL | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 19.65 |
2 | 0.12 | 22.32 |
3 | 1.05 | 20.70 |
则产品中乳酸亚铁晶体的纯度为______(以质量分数表示,保留3位有效数字)。
【答案】三颈烧瓶 2 1、3 铁粉逐渐溶解,液体中有气泡冒出、溶液变成浅绿色 3 2 Fe2++2HCO3-=FeCO3↓+CO2↑+H2O 防止FeCO3与乳酸反应产生的亚铁离子被氧化 乳酸根中羟基被酸性高锰酸钾溶液氧化 98.0%
【解析】
亚铁离子容易被氧气氧化,制备过程中应在无氧环境中进行,Fe与盐酸反应制备氯化亚铁,利用反应生成的氢气排尽装置中的空气,故B制备氯化亚铁,利用生成的氢气,使B装置中气压增大,将B装置中的氯化亚铁溶液压入C中,C装置中FeCl2和NH4HCO3发生反应:FeCl2+2NH4HCO3=FeCO3↓+2NH4Cl+CO2↑+H2O,据此解答本题。
(1)仪器C为三颈烧瓶,
故答案为:三颈烧瓶;
(2)反应前先利用生成的氢气除去装置内空气,再利用生成氢气,使B装置中气压增大,将B装置中的氯化亚铁溶液压入C中,具体操作为:关闭活塞2,打开活塞3,然后打开活塞1加入足量的盐酸,然后关闭活塞1,反应一段时间后,装置B中可观察到的现象为:铁粉逐渐溶解,液体中有气泡冒出、溶液变成浅绿色;打开活塞2,关闭活塞3;C装置中FeCl2和NH4HCO3发生反应:FeCl2+2NH4HCO3=FeCO3↓+2NH4Cl+CO2↑+H2O,反应的离子方程式为:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O,
故答案为:2;1、3;铁粉逐渐溶解,液体中有气泡冒出、溶液变成浅绿色;3;2;Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;
(3)Fe2+离子易被氧化为Fe3+离子,实验目的是制备乳酸亚铁晶体,加入Fe粉,可防止Fe2+离子被氧化,
故答案为:防止FeCO3与乳酸反应产生的亚铁离子被氧化;
(4)乳酸根中含有羟基,可以被酸性高锰酸钾溶液氧化,导致消耗高锰酸钾的增大,而计算中按亚铁离子被氧化,故计算所得乳酸亚铁的质量偏大,产品中乳酸亚铁的质量分数会大于100%,
故答案为:乳酸根中羟基被酸性高锰酸钾溶液氧化;
(5)三次滴定第二次操作消耗标准液数值明显偏大,应舍去,取第一次和第三次平均值V=![]() =19.60mL,由:Ce4++Fe2+=Ce3++Fe3+,可知25mL溶液中n(Fe2+)=n(Ce4+)=0.100mol/L×0.0196L=0.00196mol,故250mL含有n(Fe2+)=0.00196mol×
=19.60mL,由:Ce4++Fe2+=Ce3++Fe3+,可知25mL溶液中n(Fe2+)=n(Ce4+)=0.100mol/L×0.0196L=0.00196mol,故250mL含有n(Fe2+)=0.00196mol×![]() =0.0196mol,故产品中乳酸亚铁晶体的质量分数为
=0.0196mol,故产品中乳酸亚铁晶体的质量分数为![]() =98.0%,
=98.0%,
故答案为:98.0%。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标况下,22.4LCl2溶于足量水,所得溶液中Cl2、Cl-、HClO和ClO-四种微粒总数为NA
B.标准状况下,38g3H2O2中含有4NA共价键
C.常温下,将5.6g铁块投入一定量浓硝酸中,转移0.3NA电子
D.一定温度下,1L0.50mol/LNH4Cl溶液与2L0.25mol/LNH4Cl溶液含NH4+的物质的量一定不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应mA+nB![]() pC在某温度下达到平衡。
pC在某温度下达到平衡。
①若A、B、C都是气体,加压后正反应速率小于逆反应速率,则m、n、p的关系___。
②若A、B、C都是气体,且m+ n>p,而加压或升温平衡移动方向相同,则△H___0。
(2)一定条件下,将2molSO2和1molO2充入容积为2L的密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g),2分钟后反应达平衡,此时SO2的浓度为0.2mol/L,完成:
2SO3(g),2分钟后反应达平衡,此时SO2的浓度为0.2mol/L,完成:
①SO2的转化率为___。
②用O2表示的化学反应速率为__。
③平衡常数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷与氯气光照条件下取代反应的部分反应历程和能量变化如下:
第一步:![]()
第二步:![]()
第三步:![]() 中
中![]() 其中
其中![]() 表示氯原子,
表示氯原子,![]() 表示甲基
表示甲基![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A.由题可知,甲烷和氯气在室温暗处较难反应
B.![]()
C.形成![]() 中
中![]() 键放出的能量比拆开
键放出的能量比拆开![]() 中化学键吸收的能量多
中化学键吸收的能量多
D.若是甲烷与![]() 发生取代反应,则第二步反应
发生取代反应,则第二步反应![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并将产生的气体全部通过如图所示装置,得到如下表所列的实验结果(假设产生的气体完全被吸收)。

实验前 | 实验后 | |
干燥剂和U形管的质量 | 101.1 g | 102.9 g |
石灰水和广口瓶的质量 | 312.0 g | 314.2 g |
根据实验数据填空:
(1)实验完毕后,生成物中水的质量为________ g,假设广口瓶里生成一种正盐,其质量为________ g。
(2)生成的水中氢元素的质量为________ g。
(3)生成的CO2中碳元素的质量为________ g。
(4)该燃料中碳、氢元素的质量比为________。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为________,结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ag铁粉和铜粉的混合物加入到100mLbmolL-1FeCl3溶液中,固体全部溶解,再向此溶液中不断加入铁粉,当铁粉质量加至0.1ag后开始有固体析出,当铁粉加至ag时,剩余固体质量为ag。
(1)a与b的关系为___
(2)ag铁粉和铜粉的混合物中铁粉的质量为___g(用含a的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10L容器中进行如下反应:A(g)+B(g)![]() 2C(g),2分钟后,B由2mol减少到1.2mol,则用单位内A的浓度变化表示的反应速率(VA)是 ( )
2C(g),2分钟后,B由2mol减少到1.2mol,则用单位内A的浓度变化表示的反应速率(VA)是 ( )
A.0.02mol/(L·min)B.0.04mol/(L·min)
C.0.08mol/(L·min)D.0.8mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是

A. 通入保护电流使钢管桩表面腐蚀电流接近于零
B. 通电后外电路电子被强制从高硅铸铁流向钢管桩
C. 高硅铸铁的作用是作为损耗阳极材料和传递电流
D. 通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C2H6(g)![]() C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
A. 增大容器容积B. 升高反应温度
C. 分离出部分氢气D. 等容下通入惰性气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com