
过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
(1)Ca(OH)2悬浊液与H2O2溶液反应可制备CaO2·8H2O。
Ca(OH)2+H2O2+6H2O CaO2·8H2O,反应时通常加入过量的Ca(OH)2,其目的是____________。
CaO2·8H2O,反应时通常加入过量的Ca(OH)2,其目的是____________。
(2)向池塘水中加入一定里的CaO2·8H2O后,池塘水中浓度增加的离子有___________(填序号)。
A.Ca2+ B.H+ C.CO32- D.OH-
(3)CaO2在受热时能分解成CaO和O2。如图是测定样品中CaO2含量的装置。
①检查装置气密性的方法是:________________。
②加热小试管中的样品时,随着过氧化钙分解,量气瓶内的液面逐渐下降,为防止试管和量气瓶内气体压强过大,可将漏斗_______________(填“上提”或“下移”) 。

(4)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置,加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
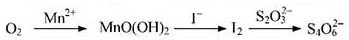
写出O2将Mn2+氧化成MnO(O H)2的离了方程式:______________。
②取加过一定量CaO2·8H2O的池塘水样l00.00ml,按上述方注测定水中溶解氧量,消耗0.01000mol/L Na2S2O3标准溶液13.50 ml.计算该水样中的溶解氧(用mg·L-1表示), 写出计算过程。
科目:高中化学 来源:2016-2017学年河北省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列变化不能用勒夏特列原理解释的是( )
A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B.H2、I2(g)混合气体加压后颜色变深
C.红棕色的NO2加压后颜色先变深再变浅
D.实验室用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上学期开学模拟化学试卷(解析版) 题型:选择题
下列实验目的无法实现的是( )
A.用激光笔光束鉴别氯化铁溶液和氢氧化铁胶体
B.用KSCN溶液鉴别Fe3+和Fe2+
C.用NaOH溶液和红色石蕊试纸鉴别溶液是否含NH4+
D.在氢氧化钠溶液中滴入氯化铁饱和溶液可以制得氢氧化铁胶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上学期期初考试化学试卷(解析版) 题型:选择题
下列关于化学反应速率的说法正确的是( )
A.反应速率是指一定时间内任何一种反应物物质的量的减少或任何一种生成物物质的量的增加
B.化学反应速率为0.8 mol·(L·s)-1是指1 s 时某物质的浓度为0.8 mol·L-1
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.对于任何化学反应来说,反应速率越快,反应现象就越明显
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上学期期初考试化学试卷(解析版) 题型:选择题
同一周期的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性顺序为:
HXO4>H2YO4>H3ZO4,则下列判断错误的是( )
A. 原子半径:X>Y>Z B. 气态氢化物的稳定性:HX>H2Y>ZH3
C. 元素原子得电子能力:X>Y>Z D. 阴离子的还原性:Z3﹣>Y2﹣>X﹣
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上学期定时训练6化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. I的原子半径大于Br, HI比HBr的热稳定性强
B. P的非金属性强于Si,H3PO4比H2SiO3的酸性强
C. Al2O3和MgO均可与NaOH溶液反应
D. SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省十堰市高一上9月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下面叙述正确的是 ( )
A.标准状况下,11.2L SO3所含分子数为0.5 NA
B.1L 1mol/L的氯化钠溶液中,所含离子数为NA
C.常温下,4.4g CO2和N2O(不反应)混合物中所含有的原子数为0.3 NA
D.一定量的铜与足量的浓硫酸反应,放出2.24L气体时,转移电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省十堰市高一上9月月考化学试卷(解析版) 题型:选择题
下列实验操作中错误的是( )
A. 在由氢氧化铜分解制氧化铜时,要边加热边用玻璃棒搅拌
B. 用药匙或者纸槽把粉末状药品送入试管的底部
C. 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
D. 如果没有试管夹,可以临时手持试管给固体或液体加热
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市宛东五校高二上第一次联考化学试卷(解析版) 题型:填空题
ⅰ.用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1160 kJ·mol-1
若用4.48 L(折合成标况体积) CH4还原NO2至N2,整个过程中转移电子总数为_________(阿伏加德罗常数的值用NA表示),放出的热量为_________kJ。
ⅱ.将1 L含有0.4 mol CuSO4和0.2 mol NaCl 的水溶液用惰性电极电解一段时间后。
(1)若在一个电极上得到0.1 mol Cu,另一电极上析出气体(在标准状况下)的体积是________L。
(2)若在一个电极上得到0.4 mol Cu,另一电极上析出气体(在标况下)的体积是_________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com