
��һ���¶��£������������ǿ��淴ӦA(g)��3B(g)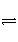
 2C(g)�ﵽƽ��״̬��־����(����)
2C(g)�ﵽƽ��״̬��־����(����)
��C���ɵ�������C�ֽ���������
�ڵ�λʱ��������amolA��ͬʱ����3amolB
��A��B��C��Ũ�Ȳ��ٱ仯
��A��B��C��ѹǿ���ٱ仯
�ݻ���������ѹǿ���ٱ仯
�����������ʵ������ٱ仯
�ߵ�λʱ��������amolA��ͬʱ����3amolB
��A��B��C�ķ�����֮��Ϊ1��3��2
A���ڢ�B���٢�C���ڢ�D���ۢ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ȷ�Ӧ���Ļ�ѧ����ʽΪ��2Al+Fe2O3 Al2O3+2Fe��ijͬѧ�ԡ����ȷ�Ӧ��������������������������Ӧ�ų��������ȣ�������ҫ�۹�â������ֽ©�����²����մ���������������ɳ�С������ġ���ѧ�ֲᡷ֪��Al��Al2O3��Fe��Fe2O3�۵㡢�е��������£�
Al2O3+2Fe��ijͬѧ�ԡ����ȷ�Ӧ��������������������������Ӧ�ų��������ȣ�������ҫ�۹�â������ֽ©�����²����մ���������������ɳ�С������ġ���ѧ�ֲᡷ֪��Al��Al2O3��Fe��Fe2O3�۵㡢�е��������£�
| ���� | Al | Al2O3 | Fe | Fe2O3 |
| �۵�/�� | 660 | 2054 | 1535 | 1462 |
| �е�/�� | 2467 | 2980 | 2750 | ﹣﹣ |
��1����ͬѧ�Ʋ⣬���ȷ�Ӧ���õ���������Ӧ�������Ͻ������Ʋ���һ���ĵ����������ǣ�����
��2�����һ����ʵ�鷽����֤���������õĿ�״�������к��н���������ʵ�������Լ������������۲쵽��������ʱ��˵���������к��н���������Ӧ�����ӷ���ʽΪ����
��3��ʵ�����ܽ����������ѡ�������Լ��е����� ������ţ���
A��Ũ���� B��ϡ���� C��ϡ���� D������������Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��18mol/L H2SO4����90mL 1.0mol/L H2SO4��
��ʵ��������A.100m L ��Ͳ B��������ƽ C�������� D.50m L����ƿ E.10m L��Ͳ F����ͷ�ι� G.50m L�ձ� H.100m L ����ƿ G.5ml��Ͳ
����ʵ��ʱѡ�õ������У�����ţ�������
���ƹ����У����������ʹ���ƽ��ƫ�ߵ��ǣ�����ţ�������
�ٶ���ʱ���ӿ̶��߹۲�Һ��
������ƿʹ��ʱδ����
�۶��ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶�
����������ƿʹ�÷����У����в�������ȷ���ǣ�����ţ�����
A��ʹ������ƿǰ������Ƿ�©ˮ��
B������ƿ������ˮϴ�������ô���Һ��ϴ��
C��������Һʱ����������ǹ��壬�ѳƺõ�������ֽ��С�ĵ�������ƿ�У�������������ˮ���ӽ��̶���1��2cm�����ٸ��ý�ͷ�ιܼ�����ˮ���̶��ߣ�
D��������Һʱ�����������Һ�壬����Ͳ��ȡ������ֱ�ӵ�������ƿ�У�������������ˮ���ӽ��̶�����1��2cm�����ٸ��ý�ͷ�ιܼ�����ˮ���̶��ߣ�
E�����ݺǺ�ƿ������ʳָ��סƿ��������һֻ�ֵ���ָ��סƿ�ף�������ƿ��ת��ҡ�ȣ�
F��������100mL0.200mol/L���Ȼ�����Һʱ���ɽ��������Ȼ��ƹ�������100mL����ˮ�У�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��ӦA2(g)��2B2(g)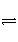
 2AB2(g)����H<0������˵����ȷ����(����)
2AB2(g)����H<0������˵����ȷ����(����)
A�������¶ȣ�����Ӧ�������ӣ�����Ӧ���ʼ�С
B�������¶������ڷ�Ӧ�������ӣ��Ӷ����̴ﵽƽ���ʱ��
C���ﵽƽ��������¶Ȼ�����ѹǿ�������ڸ÷�Ӧƽ�������ƶ�
D���ﵽƽ������¶Ȼ��Сѹǿ�������ڸ÷�Ӧƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

��֪ij���淴ӦmA(g)��nB(g)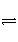
 pC(g)���ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��tʱ���¶�T��ѹǿp�뷴Ӧ��B�ڻ�������е��������B%�Ĺ�ϵ���ߣ������߷����������ж���ȷ����(����)
pC(g)���ܱ������н��У���ͼ��ʾ�ڲ�ͬ��Ӧʱ��tʱ���¶�T��ѹǿp�뷴Ӧ��B�ڻ�������е��������B%�Ĺ�ϵ���ߣ������߷����������ж���ȷ����(����)
A��T1<T2��p1>p2��m��n>p�����ȷ�Ӧ
B��T1>T2��p1<p2��m��n>p�����ȷ�Ӧ
C��T1<T2��p1>p2��m��n<p�����ȷ�Ӧ
D��T1>T2��p1<p2��m��n<p�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2L���ܱ������ڣ�800��ʱ��Ӧ2NO(g)��O2(g)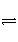
 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1) д���÷�Ӧ��ƽ�ⳣ������ʽ��K��_____________________________________��
��֪��K300��>K350������÷�Ӧ��______�ȷ�Ӧ��
(2)��ͼ��ʾNO2�ı仯��������__________����O2��ʾ��0��2s�ڸ÷�Ӧ��ƽ������v��_____________________________________
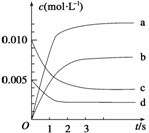
(3)��˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2)
b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2)
d���������ܶȱ��ֲ���
(4)Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����________������������������������������������
a����ʱ�����NO2����b���ʵ������¶�c������O2��Ũ��d��ѡ���Ч����
�����⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ײ��ϡ�������ֱ��Ϊ1nm��100nm�IJ��ϣ�����̼�������е�һ�֣�ij�о���������̼���ȵķ�ɢ������ˮ�У��õ������ʢ�����Һ ���ǽ��� �۾��ж�������� �ܲ�������Ĥ �ݲ�������ֽ ��ֹ�����ֺ�ɫ������
������ȷ���ǣ�������
| �� | A�� | �٢ܢ� | B�� | �ڢۢ� | C�� | �ڢۢ� | D�� | �٢ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����������״̬�����ʢٸɱ� ��NaCl���� �۰�ˮ �ܴ��� �ݾƾ�ˮ��Һ ��ͭ �����ڵ�KOH �����ǣ��������ڵ���ʵ�������������ţ������ڷǵ���ʵ�������������ţ����ܵ����������������ţ���
��2��ij��ɫ�������Һ�У����ܴ���������Ag+��H+��Cu2+��OH﹣��Cl﹣�����ӣ�����Ϊ��һ���е�������������һ��û�е�����������������ȷ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1.01KPa��298K�����£�2molH2����ˮ�����ų�484kJ�����������Ȼ�ѧ����ʽ��ȷ���ǣ�������
�� A�� 2H2��g��+O2��g��=2H2O��l������H=﹣484kJ/mol
�� B�� H2O��g��=H2��g��+ O2��g������H=﹣242kJ/mol
O2��g������H=﹣242kJ/mol
�� C�� 2H2��g��+O2��g��=2H2O��g������H=+484kJ/mol
�� D�� H2��g��+ O2��g��=H2O��g������H=﹣242kJ/mol
O2��g��=H2O��g������H=﹣242kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com