
| A. | 9种 | B. | 15种 | C. | 45种 | D. | 50种 |
分析 -C3H6Cl是用一个氯原子取代了丙基中的一个-H,故-C3H6Cl的结构有5种;分子式为C8H10的芳香烃,可能是乙苯,还可能是二甲苯,而根据2个甲基在苯环上的位置关系,可能是邻二甲苯、间二甲苯或对二甲苯,苯环的氢原子有几种,则被-C3H6Cl取代的位置就有几种,据此分析.
解答 解:-C3H6Cl是用一个氯原子取代了丙基中的一个-H,故-C3H6Cl的结构有5种:-CHClCH2CH3,-CH2CHClCH3,-CH2CH2CH2Cl,-CH(CH2Cl)CH3,-CCl(CH3)2.
分子式为C8H10的芳香烃,可能是乙苯、邻二甲苯、间二甲苯或对二甲苯.
若为乙苯,则苯环上打的氢原子有5种,则被-C3H6Cl取代的位置有3种,故所得的同分异构体为3×5=15种;
若为邻二甲苯,则苯环上的氢原子有2种,则被-C3H6Cl取代的位置有2种,故所得的同分异构体为2×5=10种;
若为间二甲苯,则苯环上的氢原子有3种,则被-C3H6Cl取代的位置有3种,故所得的同分异构体为3×5=15种;
若为对二甲苯,则苯环上的氢原子有1种,则被-C3H6Cl取代的位置有1种,故所得的同分异构体为1×5=5种;
故所得的同分异构体共有45种.
故选C.
点评 本题考查了同分异构体的书写,应注意的是物质中有几种氢原子,则一取代产物就有几种.难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 室温时,1L pH=2的NH4Cl溶液中水电离出10-12 molH+ | |
| B. | 常温常压下,46g NO2含有的原子数等于3NA | |
| C. | 12g石墨含有4NA个自由移动的电子 | |
| D. | 22.4LCl2与足量NaOH反应,转移电子数NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
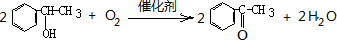 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
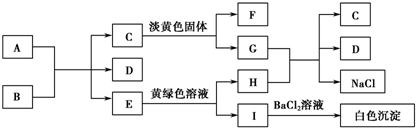
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
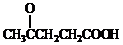 )合成聚芳酯E的路线(省略部分产物):
)合成聚芳酯E的路线(省略部分产物):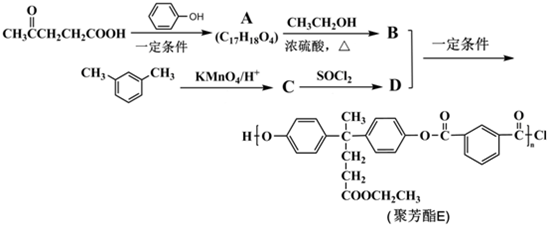
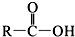 +SOCl2→
+SOCl2→ +SO2+HCl
+SO2+HCl +R′OH→
+R′OH→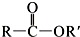 +HCl(R、R′表示烃基)
+HCl(R、R′表示烃基)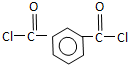 .
.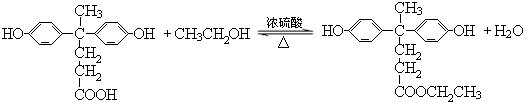 ,.
,.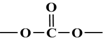 结构写出F与足量NaOH溶液共热反应的化学方程式:
结构写出F与足量NaOH溶液共热反应的化学方程式: .
.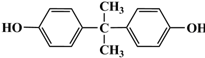 的路线.
的路线.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (R、R′代表烃基)
(R、R′代表烃基)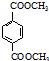 有多种同分异构体,同时满足下列条件的同分异构体有8种.
有多种同分异构体,同时满足下列条件的同分异构体有8种. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | |||||||||||||||
| ⑨ | ⑩ |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
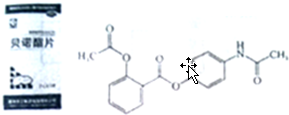
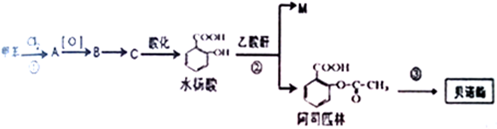
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com