
下列叙述正确的是( )
A.1mol NaCl中含有6.02×1023个NaCl分子
B.欲配制1L1mol.L-1的NaCl溶液,可将 58.5gNaCl溶于 1L水
C.含有2×6.02×1023个阴离子的CaC2,在标准状况下能产生约44.8L的乙炔气体
D.1molCl2与足量的铁反应,转移的电子数为3×6.02×1023
科目:高中化学 来源: 题型:
甲、乙两池的电极材料如图所示,请按要求回答下列问题:

(1)若两池中均为Cu(NO3)2溶液,反应一段时间后:
①有红色物质析出的是甲池中的 (填“铁”或“碳”)棒;乙池中的 (填“阴”或“阳”)极。
②乙池中阳极上发生的电极反应方程式是 。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的化学方程式: 。
②甲池中碳极上电极反应方程式是 ,乙池碳极上
电极反应属于 (填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙池碳极附近,发现试纸变蓝,待一段时间后又发现
蓝色褪去。这是因为过量的Cl2将生成的I2又氧化。若反应的C12和I2物质的量
之比为5:1,且生成HCl和另一种强酸,该强酸的化学式为 。
④若乙池中转移0.1 mol e-后停止实验,池中溶液体积是1L,则溶液混匀后的pH= (不考虑所生成的气体溶解在溶液中的情况)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各表述与示意图一致的是

A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2 (g) + O2(g)  2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化
2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)→CH3CH3(g) ΔH<0使用(a)和未使用(b)催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇被称21世纪的新型燃料,工业上通过下列反应(Ⅰ)和(Ⅱ),用CH4和H2O为原料来制备甲醇。
(1)将1.0 mol CH4和一定量H2O(g)通入反应室(容积为10 L),在一定条件下发生反应:
CH4(g)+H2O(g) 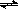 CO(g)+3H2(g) ΔH=QkJ/mol (Ⅰ)
CO(g)+3H2(g) ΔH=QkJ/mol (Ⅰ)
CH4的转化率与温度、压强的关系如下图。

①图中的p1____p2(填“<”、“>”或“=”下同),且Q 0;
②该反应的平衡常数表达式为 ;
③100℃,p1压强下,该反应达到平衡时,H2O 的转化率为20%,则最初加入H2O(g)的物质的量为 。
(2)200℃压强为0.1 MPa条件下,将CO、H2混合后在催化剂作用下能反应生成甲醇:
CO(g)+2H2(g) 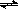 CH3OH(g) ΔH=−84kJ/mol (Ⅱ)
CH3OH(g) ΔH=−84kJ/mol (Ⅱ)
①在上述条件下,将1molCO、3molH2混合后在容积为5L的密闭容器中充分反应后,放出热量21 kJ,则该条件下其化学平衡常数为 ;
②在上述条件下,将1mol CH3OH(g)在相同密闭容器中反应达平衡后,与上述平衡相比,下列说法正确的是 。
A.CO体积分数更大 B.c(CH3OH)更大
C.化学平衡常数减小 D.吸收热量>63kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.某醋酸溶液的pH=a,将此溶液稀释100倍后,溶液的pH=b,则a=b+2
B.在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7
C.1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0
D.常温下,若1 mL pH=1的盐酸与100 mL NaOH溶液混合后,溶液的pH=7则NaOH溶液的pH=11
查看答案和解析>>
科目:高中化学 来源: 题型:
3.04g铜镁合金完全溶解于含 的浓HNO3中,得到NO2和N2O4混合气2240mL(标
的浓HNO3中,得到NO2和N2O4混合气2240mL(标
准状况下)。向反应后的溶液中加入2mol L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀,下列说法不正确的是( )
L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀,下列说法不正确的是( )
①该合金中镁与铜的物质的量之比为1:2
②NO2和N2O4的混合气体中,N2O4的体积分数为80%
③得到5.08g沉淀时,加入NaOH溶液的体积是620mL
④该反应中共转移电子为1.2NA
A.③ B.②③④ C.①③ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是( )

A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ
C.该反应达到平衡态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ
D.同一种反应物在平衡态Ⅰ和平衡态Ⅱ时浓度不相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com