
【题目】某学生利用下面实验装置探究盐桥式原电池的工作原理。按照实验步骤依次回答下列问题:

(1)铜为___极,导线中电子流向为___(用a、b表示)。
(2)若装置中铜电极的质量增加3.2g,则导线中转移的电子数目为___;(用若NA表示阿伏加德罗常数,“NA”表示)
(3)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向的表述正确的是___。
A.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动
B.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动
C.盐桥中的K+、Cl-几乎都不移动
(4)若将反应2Fe3+ +Cu=2Fe2+ +Cu2+设计成原电池,其正极反应是___。
(5)设计一个电化学装置,实现这个反应:Cu+H2SO4=CuSO4+H2↑,请在下面方框内画出这个电化学装置图。___

【答案】正 a→b 0.1NA A Fe3+ +e— =Fe2+ 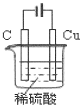
【解析】
(1)锌铜原电池中,锌比铜活泼,故锌为负极,铜为正极;原电池中,电子由负极流向正极,故电子的流向为a→b;
(2)3.2g铜物质的量为0.05mol,由电极反应式Cu2++2e-=Cu可知,生成1mol铜,转移2mol电子,故生成0.05mol铜,导线中转移0.1mol电子,电子数目为0.1NA;
(3)左侧烧杯中锌失电子变成锌离子,使得锌电极附近带正电荷,吸引阴离子向左侧烧杯移动,右侧烧杯中铜离子得到电子变成铜,使得铜电极附近带负电荷,吸引阳离子向右侧烧杯移动,故盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动;
故答案为A;
(4)根据方程式2Fe3++Cu=Cu2++2Fe2+可知氧化剂是铁离子,还原剂是铜,所以如果设计成原电池,负极应该是铜,正极是石墨或金属性弱于铜的金属,铁离子在正极放电,则正极反应为Fe3+ +e- =Fe2+;
(5)Cu+H2SO4(稀)=CuSO4+H2↑不能自发发生,应设计为电解池,Cu失去电子,为阳极,阴极材料任意,而电解质为硫酸,若阴极为C棒,则电解装置为 。
。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】阅读下面的信息,推断元素及有关物质,按要求回答物质:
信息①:X、Y、Z、W是常见的短周期元素,其原子序数依次增大,且原子核外最外层电子数均不少于2。
(1)根据信息①:X一定不是_________(填序号).
A.氢 | B.碳 | C.氧 | D.硫 |
信息②:上述四种元素的单质均能在足量的氧气中燃烧,生成的四种氧化物中,有两种能溶
于稀硫酸,三种能溶于浓氢氧化钠溶液,氧化物的相对分子质量都大于26。
(2)这四种元素中是否可能有一种是铝元素?_____________________________________。
信息③:向上述四种元素单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤,向
滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀。
(3)白色沉淀物的化学式为____________________________________________________。
信息④:向上述四种元素单质组成的混合物中加入足量烧碱溶液,固体部分溶解,过滤,向
滤液中加入过量的盐酸溶液,最终溶液中析出白色沉淀。
(4)生成白色沉淀物的离子方程式为____________________________________________。
信息⑤:X与W同主族
(5)X与浓硫酸加热时反应的化学方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法不正确的是( )

A.元素甲的原子结构示意图为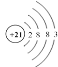
B.原子半径比较:甲>乙>Si
C.元素乙的简单气态氢化物的稳定性比CH4弱
D.推测乙可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置是化学实验室的常用装置,它有多种用途.以下各项用途和操作都正确的是
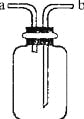
(已知:2H2S+SO2=3S+2H2O)
A.干燥CO2:瓶内放一定体积浓硫酸,由a进气
B.用于收集O2:瓶内充满水,由b进气
C.提供少量CO:瓶内充满CO,b接进水管
D.用做H2S和SO2反应的装置:由a通入H2S,b通入SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴可逆反应FeO(s)+CO(g)Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
T/K | 938 | 1100 |
K | 0.68 | 0.40 |
①写出该反应平衡常数的表达式________。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量________;充入氦气,混合气体的密度________(填“增大”“减小”或“不变”)。
⑵常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①根据表中数据判断,浓度均为0.01 mol·L-1的下列四种物质的溶液中,酸性最强的是________ (填编号)。
A.HCN B.HClO C.H2CO3 D.CH3COOH
②据上表数据,请你判断下列反应不能成立的是________(填编号)。
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN C.CO2+H2O+2NaClO=Na2CO3+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molCO和3molH2O混合于2L的密闭容器中,发生如下可逆反应:CO(g)+H2O(g)![]() CO2(g)+H2(g);
CO2(g)+H2(g);
(1)该化学反应的平衡常数表达式:___。
(2)已知在700℃时,该反应的平衡常数K1=2,则该温度下反应CO2(g)+H2(g)CO(g)+H2O(g)的平衡常数K2=__,反应2CO(g)+2H2O(g)2CO2(g)+2H2(g)的平衡常数K3=___。
(3)已知在1000℃时,该反应的平衡常数K4=1.0,则该反应为___反应(填“吸热”或“放热”),△H__0(填“>”或“<”)。
(4)在1000℃下,某时刻CO2的物质的量为1mol,则此时υ(正)__υ(逆)(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是
A.甲装置:可用来证明碳酸的酸性比硅酸强
B.乙装置:可用来检验二氧化硫气体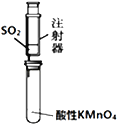
C.丙装置:用图示的方法不能检查此装置的气密性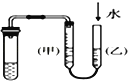
D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气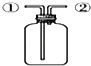
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家刚刚发现了某种元素的原子,其质量是ag,一个12C的原子质量是bg,NA是阿伏加德罗常数的值,下列说法不正确的是( )
A.该原子的摩尔质量是aNAg/mol
B.Wg该原子的物质的量是![]() mol
mol
C.该原子的相对原子质量为![]()
D.由已知信息可得NA=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是( )
A.与NaOH反应的氯气为0.25 mol
B.n(Na+):n(Cl-) 可能为7:3
C.若反应中转移的电子为n mol,则0.15n0.25
D.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com