
 在下列化合物中:H2O2 、Na2O、、I2 、、NaCl、、CO2、NH4Cl、Na2O2,用化学式回答下列问题:
在下列化合物中:H2O2 、Na2O、、I2 、、NaCl、、CO2、NH4Cl、Na2O2,用化学式回答下列问题: 只由非金属组成的离子化合物是 ,
只由非金属组成的离子化合物是 , 只含有非极性共价键的是 ,
只含有非极性共价键的是 ,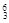 Li ②
Li ②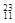 Na ③
Na ③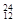 Mg ④
Mg ④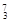 Li ⑤
Li ⑤ C ⑥C60 ⑦石墨,为同位素的是 ,互为同素异形体的是 。(填编号)
C ⑥C60 ⑦石墨,为同位素的是 ,互为同素异形体的是 。(填编号)科目:高中化学 来源:不详 题型:单选题
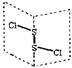
| A.S2Cl2的结构式为Cl-S-S-Cl |
| B.若S2Br2与S2Cl2结构相似,则熔沸点:S2Br2>S2Cl2 |
| C.S2Cl2为含有极性键和非极性键的非极性分子 |
| D.S2Cl2与H2O反应的化学方程式可能为: 2S2Cl2 + 2H2O → SO2↑ + 3S↓ + 4HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.O2、O3、O4都是氧的同素异形体 | B.O2、O3、O4都是氧的同位素 |
| C.O4的摩尔质量为64 | D.O2、O3、O4都互称为同分异构体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
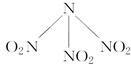
| A.分子中N、O间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该分子中的中心氮原子采取sp3杂化 |
| D.15.2 g该物质含有6.02×1022个原子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
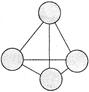
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电负性最大的原子价电子构型:3S23p5 |
| B.N3-、CO2和O3互为等电子体,所以它们空间构型都是直线型 |
| C.共价键和离子键都既有方向性又有饱和性 |
| D.根据VSEPR理论判断SF6空间构型为 正八面体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com