


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
| A、FeCl3与氨水反应:Fe3++3NH3?H2O═Fe(OH)3↓+3NH4+ |
| B、铜与稀硝酸反应:Cu+8H++2NO3-═Cu2++2NO↑+4H2O |
| C、NO2与水反应:3NO2+H2O═NO3-+NO+2H+ |
| D、醋酸与CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
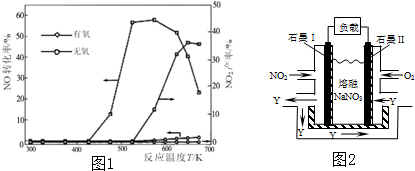
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 将一定质量的镁和铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5mol?L-1 NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.请通过计算回答:
将一定质量的镁和铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5mol?L-1 NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.请通过计算回答:查看答案和解析>>
科目:高中化学 来源: 题型:
 如图1所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的N2和H2使三容器压强相等,一定条件下发生N2+3H2?2NH3的反应.问:
如图1所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的N2和H2使三容器压强相等,一定条件下发生N2+3H2?2NH3的反应.问:查看答案和解析>>
科目:高中化学 来源: 题型:
 已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl、HCl、H2O、NaOH |
| B、Cl2、Na2S、HF、SO2 |
| C、HBr、CO2、NH3、H2O |
| D、Na2O2、H2O2、O3、CH4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com