
分析 A的二氯取代物是D,D有两种同分异构体,故D只能为CH3CHCl2或CH2ClCH2Cl;可知A为CH3CH3,B与溴的四氯化碳溶液可以发生加成反应,为烯烃,与A的碳原子数相等,则B为CH2=CH2,加成产物是E,故E为BrCH2CH2Br;E只有一种同分异构体C,故C为CH3CHBr2,以此解答该题.
解答 解:A的二氯取代物是D,D有两种同分异构体,故D只能为CH3CHCl2或CH2ClCH2Cl;可知A为CH3CH3,B与溴的四氯化碳溶液可以发生加成反应,为烯烃,与A的碳原子数相等,则B为CH2=CH2,加成产物是E,故E为BrCH2CH2Br;E只有一种同分异构体C,故C为CH3CHBr2,
故答案为:A:CH3CH3;B:CH2=CH2;C:CH3CHBr2;D:CH3CHCl2(或者CH2ClCH2Cl);E:CH2BrCH2Br.
点评 本题考查有机物的推断,是高考中的常见题型,属于中等难度的试题.试题综合性强,贴近高考.在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养.旨在培养学生分析、归纳、总结问题的能力.有利于培养学生的逻辑推理能力和创新思维能力.D的推断为解答该题的关键,注意把握题给信息.


科目:高中化学 来源: 题型:选择题
| A. | 浓碱飞溅到皮肤上,应立刻涂上硫酸溶液 | |
| B. | 金属钠着火,立刻用泡沫灭火器扑灭 | |
| C. | 加热试管时,先来回移动酒精灯加热,再对准药品集中加热 | |
| D. | 用天平称量固体药品时,砝码放在左盘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+的结构示意图为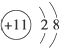 | |
| B. | 明矾的化学式为KAl(SO4)2•12H2O | |
| C. | 某微粒的电子数等于质子数,则该微粒可能是分子或离子 | |
| D. | 化学变化不产生新元素,产生新元素的变化不是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
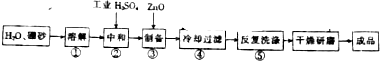
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
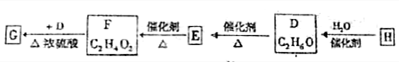

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一定量KAl(SO4)2溶液和一定量Ba(OH)2溶液混合,沉淀的质量恰好最大时:Al3++2SO42-+3OH-+2Ba2+═2BaSO4↓+Al(OH)3↓ | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ | |
| D. | 用Al(OH)3中和过多的胃酸:Al(OH)3+3H+═Al3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com