
【题目】有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式 .
(2)B元素在周期表中的位置;离子半径:BA(填“大于”或“小于”).
(3)C原子的电子排布图是 , 其原子核外有个未成对电子,能量最高的电子为轨道上的电子,其轨道呈形.
(4)D原子的电子排布式为 , D﹣的结构示意图是 .
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为与D的氢化物的水化物反应的化学方程式为 .
【答案】
(1)1s22s22p63s1
(2)第三周期第ⅢA族;小于
(3)![]() ;3;2p;哑铃
;3;2p;哑铃
(4)1s22s22p63s23p5或[Ne]3s23p5;
(5)Al(OH)3+3HClO4═Al(ClO4)3+3H2O;3HCl+Al(OH)3═AlCl3+3H2O
【解析】解:A是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂,所以A为Na元素;B与A同周期,其最高价氧化物的水化物呈两性,则B为Al元素;C元素的气态氢化物极易溶于水,可用作制冷剂,则C为N元素;D是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,则D为Cl元素,(1)A为钠元素,A原子的核外电子排布式1s22s22p63s1 , 故答案为:1s22s22p63s1;(2)B为铝元素,B元素在周期表中的位置第三周期第ⅢA族,电子层数相同的离子,核电荷数越大,离子半径半径越小,所以铝离子半径小于钠离子,
故答案为:第三周期第ⅢA族;小于;(3)C为氮元素,C原子的基态原子的电子排布图是 ![]() ,其原子核外有3个未成对电子,能量最高的电子为2p轨道上的电子,其轨道呈哑铃,
,其原子核外有3个未成对电子,能量最高的电子为2p轨道上的电子,其轨道呈哑铃,
故答案为: ![]() ;3;2p;哑铃;(4)D为氯元素,氯原子核外电子排布式为:1s22s22p63s23p5或[Ne]3s23p5;Cl﹣的结构示意图为
;3;2p;哑铃;(4)D为氯元素,氯原子核外电子排布式为:1s22s22p63s23p5或[Ne]3s23p5;Cl﹣的结构示意图为  ,
,
故答案为:1s22s22p63s23p5或[Ne]3s23p5;  ; (5)B为铝元素,D为氯元素,B的最高价氧化物对应的水化物与D的最高价氧化物的水化物反应的化学方程式为:Al(OH)3+3HClO4═Al(ClO4)3+3H2O;D的氢化物HCl,氯化氢与氢氧化铝反应的离子方程式为:3HCl+Al(OH)3═AlCl3+3H2O,
; (5)B为铝元素,D为氯元素,B的最高价氧化物对应的水化物与D的最高价氧化物的水化物反应的化学方程式为:Al(OH)3+3HClO4═Al(ClO4)3+3H2O;D的氢化物HCl,氯化氢与氢氧化铝反应的离子方程式为:3HCl+Al(OH)3═AlCl3+3H2O,
故答案为:Al(OH)3+3HClO4═Al(ClO4)3+3H2O;3HCl+Al(OH)3═AlCl3+3H2O.
A是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂,所以A为Na元素;
B与A同周期,其最高价氧化物的水化物呈两性,则B为Al元素;
C元素的气态氢化物极易溶于水,可用作制冷剂,则C为N元素;
D是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,则D为Cl元素,据此进行答题.


科目:高中化学 来源: 题型:
【题目】某同学用下图所示的装置及药品进行比较酸性强弱的实验,一段时间后试管②中有胶冻状物质生成。下列说法正确的是( )
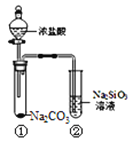
A. 用带有玻璃塞的试剂瓶盛装Na2SiO3溶液
B. 试管①中反应的离子方程式是:Na2CO3+ 2H+ = 2Na+ + CO2↑+ H2O
C. 该实验可以证明酸性:盐酸>碳酸>硅酸
D. 若将盐酸换成硫酸,能证明酸性:硫酸>碳酸>硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题:
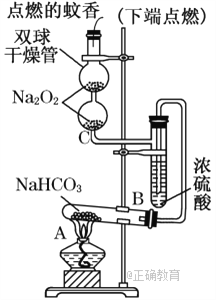
(1)在A试管内发生反应的化学方程式是____________________________________.
(2)B装置的作用是_______________________________________________________.
(3)在双球干燥管内发生反应的化学方程式为___________________________________.
(4)双球干燥管内观察到的实验现象是_________________________________________.上述实验现象说明________________________________________________________.
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是______________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl-浓度最小的是 ( )
A. 1000mL 2.5mol/L NaCl溶液 B. 200mL 2mol/L MgCl2溶液
C. 300mL 5mol/L KCl溶液 D. 250mL 1mol/L AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同元素的原子在分子内吸引电子的能力大小可用一数值X来表示,若X越大,则原子吸引电子的能力越强,在所形成的分子中成为负电荷一方.下面是某些短周期元素的X值.
元素 | Li | Be | B | C | O | F |
X值 | 0.98 | 1.57 | 2.04 | 2.53 | 3.44 | 3.98 |
元素 | Na | Al | Si | P | S | Cl |
X值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析X值的变化规律,确定N、Mg的X值范围:<X(Mg)<; <X(N)< .
(2)推测X值与原子半径的关系是 .
(3)某有机物结构简式为 ![]() ,在S~N中,你认为共用电子对偏向谁?(写原子名称).
,在S~N中,你认为共用电子对偏向谁?(写原子名称).
(4)经验规律告诉我们当成键的两原子相应元素电负性的差值△X>1.7时,一般为离子键,当△X<1.7时,一般为共价键,试推断AlBr3中化学键的类型是
(5)预测元素周期表中,X值最小的元素位置(放射性元素除外).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是
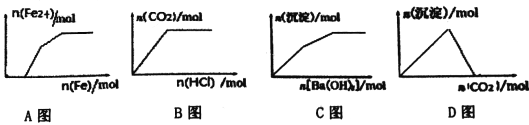
A. Fe(NO3)3、Cu(NO3)2、HNO3混合溶液中逐渐加入铁粉
B. Na2CO3、NaHCO3溶液中逐滴加入HCl
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液
D. NaAlO2溶液中逐渐通入CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。下列说法正确的是
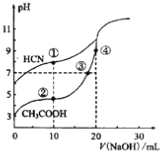
A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
C. 点④所示溶液液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )
A. 浓硫酸的体积增大
B. 铝的表面生成致密的氧化膜
C. 澄清的石灰水变浑浊
D. 氢氧化钠的表面发生潮解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.煤、石油、天然气是当今世界最重要的三种化石燃料
B.CaO+H2O=Ca(OH)2可放出大量热,可利用该反应设计成原电池,把化学能转化为电能
C.决定化学反应速率的主要因素为反应温度
D.人体运动所消耗的能量与化学反应无关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com