
| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/ | 0.44 | 0.6 | 0.6 |
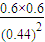 =1.86��400����Ӧ������Ӧ������У�����v����v����
=1.86��400����Ӧ������Ӧ������У�����v����v����

 ����ѧ���ʱѧ����ϵ�д�
����ѧ���ʱѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
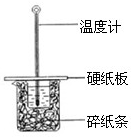 ��1�����ⶨ��20g������������ȼ������ˮ����������2418.0kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ
��1�����ⶨ��20g������������ȼ������ˮ����������2418.0kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | CH3OH | CH3OCH3 | H2O |
| Ũ��/��mol?L-1�� | 0.44 | 0.6 | 0.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��ӱ�ʡ�������и߶���ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��14�֣���Ӧ3Fe��S��+4H2O====Fe3O4��s��+4H2��g������һ�ɱ���ݻ����ܱ������н��У��Իش�
��1������Fe������������Ӧ���ʵı仯�� ���������䡢��С��������ͬ��
��2���������������Сһ�룬������Ӧ���� ���淴Ӧ���� ��
��3������������䣬����N2ʹ��ϵѹǿ����������Ӧ���� ���淴Ӧ���� ��
��4������ѹǿ���䣬����N2ʹ�������������������Ӧ���� �淴Ӧ���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com