
(14分)高锰酸钾广泛用作氧化剂、防腐剂、消毒剂、除臭剂及解毒剂。常见的制备流程如下:
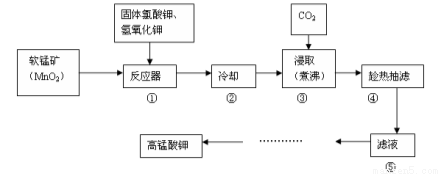
已知:a.3MnO2+KClO3+6KOH=3K2MnO4+KCl+3H2O B.3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
请回答下列问题:
(1)步骤①中反应所选用的坩埚不能用 。
A.石英坩埚 B.铁坩埚 C.瓷坩埚 D.石墨坩埚
(2)步骤③通CO2的目的是为了调节溶液的pH,能否改用氯化氢 (填“能”或“否”),原因是 。
(3)步骤④中抽滤得到的固体是 。
(4)抽滤装置主要由 、安全瓶、抽气泵和布氏漏斗四部分组成,该实验中抽滤时能否用滤纸?______(填“能”或“不能”), 理由是_____。
(5)从滤液⑤得到高锰酸钾的后续操作步骤是____。
(1)AC;
(2)否,反应生成的高锰酸钾能被HCl还原,产生的氯气有毒,污染环境。
(3)二氧化锰。
(4)吸滤瓶,不能,因为高锰酸钾具有强氧化性,能腐蚀滤纸。
(5)蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
【解析】
试题分析:(1)根据题给工艺流程图知,步骤①中有氢氧化钾参加反应,A、石英坩埚的成分为二氧化硅,C、瓷坩埚中含有二氧化硅,与氢氧化钾反应,不能选用,选AC;(2)结合题给信息和高锰酸钾和盐酸的性质分析。步骤③通CO2的目的是为了调节溶液的pH,不能改用氯化氢,原因是反应生成的高锰酸钾能被HCl还原,产生的氯气有毒,污染环境。(3)步骤④中抽滤得到的固体是二氧化锰。(4)抽滤装置主要由吸滤瓶、安全瓶、抽气泵和布氏漏斗四部分组成,该实验中抽滤时不能用滤纸,理由是因为高锰酸钾具有强氧化性,能腐蚀滤纸。(5)从滤液⑤得到高锰酸钾的后续操作步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
考点:以高锰酸钾制备的工艺流程为载体考查相关物质的性质及分离、化学实验基本操作等。


科目:高中化学 来源:2013-2014湖北省大冶市春季期末考试高二化学试卷(解析版) 题型:填空题
(1 5分)
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或受热。实验室以电解法制备ClO2的流程如下:
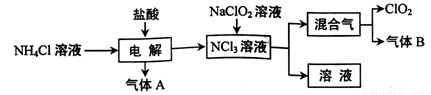
(1)ClO2中所有原子 (填“是”或“不是”)都满足8电子结构。上图所示方法制得的混合气中杂质气体B能使石蕊试液显蓝色,除去该杂质气体可选用 __;
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品。下列说法正确的是 ;
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备,但该方法缺点是产率低、产品难以分离,还可能污染环境。写出该方法发生的化学方程式 ;
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是
,此法相比欧洲方法的优点是 。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为 ,此法提高了生产及储存、运输的安全性,原因是____ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014海口市第二学期高二化学期中考试(B卷)试卷(解析版) 题型:填空题
(14分)某有机物X(C12H14O7)的分子中含有多种官能团,其结构简式为:

(其中R1、R2为未知部分的结构),已知X可以发生如图所示的转化:
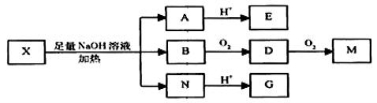
已知1)向X、E的水溶液中滴入FeCl3溶液均发生显色反应; 2)E的核磁共振谱图中只有两个峰,面积比为1:2; 3)G、M(C2H2O4)都能与NaHCO3溶液反应。
(1)写出X的结构简式为 。
(2)1molX与NaOH溶液反应时,消耗 mol NaOH。
(3)E的结构简式是 ;B的命名为_____________________
①写出B转化成D的化学方程式:___________ __________
②写出A溶液与CO2反应的离子方程式:________________ _________。
H与G互为同分异构体,H的分子中只含有醛基、羧基、羟基三种官能团,且同一个碳原子上不 能同 时连有两个羟基,则H的分子结构有______种.
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省绍兴市柯桥区高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
(14分)中药葛根是常用祛风解表药物,其有效成分为葛根大豆苷元,用于治疗高血压引起的头疼、头晕、突发性耳聋等症。其合成线路如下:
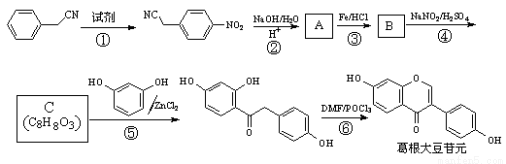
已知:
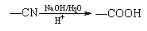 ;
; 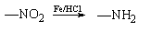
请回答以下问题:
(1)物质C的结构简式为
(2)对于葛根大豆苷元,下列说法正确的是
A.1 mol葛根大豆苷元最多可以和2 molNaOH反应 B.不发生硝化反应
C.可发生水解反应 D.与溴水可发生加成或取代反应
(3)步骤①变化所需加的试剂是 ,步骤③的反应类型为
(4)物质B发生缩聚反应生成高分子化合物的反应方程式为
(5)写出同时符合下列条件的物质C同分异构体的结构简式 (写一种)
i.不能与Fe3+发生显色反应 ii. 可以发生银镜反应
iii.苯环上有两种不同化学环境的氢原子
(6)有以下合成线路:
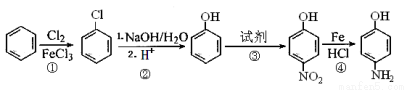
请结合所学知识和题给信息,分析上述合成线路的合理性上存在的问题
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省绍兴市柯桥区高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
X、Y、Z、W为短周期元素,原子半径X>Y>Z>W,X、Y、Z处于同一周期,Z、W处于同一主族,X、Y、Z原子序数之和为40,X是短周期中除稀有气体元素外半径最大的元素。下列说法正确的是
A.若X、Y、W形成的化合物为XYW2,则其水溶液可以显碱性
B.Y的最高价氧化物对应的水化物一定是碱
C.稳定性:W的氢化物>Z的氢化物,沸点:Z的氢化物>W的氢化物
D.X、Y的氧化物晶体类型一定相同
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高三下学期联考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.按系统命名法, 有机物(CH3)2CHCH(CH2CH3)(CH2CH2CH3)的名称是:2-甲基-3-丙基戊烷
B. 分子中所有原子共平面
分子中所有原子共平面
C.某蔗糖酯可以由蔗糖与硬脂酸乙酯合成,反应如下:
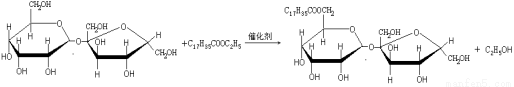
该蔗糖酯在稀硫酸的作用下水解能得到三种有机产物
D.荧光黄的结构简式为 ,其分子式为C20H12O5,理论上1mol该有机物最多消耗2molNaOH,并能与双缩脲试剂发生显色反应
,其分子式为C20H12O5,理论上1mol该有机物最多消耗2molNaOH,并能与双缩脲试剂发生显色反应
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省湖州市高三二模理综化学试卷(解析版) 题型:简答题
(14分)研究CO2与CH4的反应使之转化为CO和H2,对减缓燃料危机,减少温室效应具有重要的意义。
(1)已知:①2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) △H=-484kJ·mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802kJ·mol-1
则CH4(g)+CO2(g) 2CO(g)+2H2(g) △H= kJ·mol-1
2CO(g)+2H2(g) △H= kJ·mol-1
(2)在密闭容器中通入物质的量浓度均为0.1mol·L-1的CH4与CO2,在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。

?据图可知,P1 、P2、 P3 、P4 由大到小的顺序 。
?在压强为P4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为 。该温度下,反应的平衡常数为 。
(3)CO和H2在工业上还可以通过反应C(s)+H2O(g)  CO(g)+H2 (g)来制取。
CO(g)+H2 (g)来制取。
①在恒温恒容下,如果从反应物出发建立平衡,可认定平衡已达到的是
A.体系压强不再变化 B.H2与CO的物质的量之比为1 :1
C.混合气体的密度保持不变 D. 气体平均相对分子质量为15,且保持不变
② 在某密闭容器中同时投入四种物质,2min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、
2.2molH2(g)和一定量的C(s),如果此时对体系加压,平衡向 (填“正”或“逆”)反应方向移动,第5min时达到新的平衡,请在下图中画出2~5min内容器中气体平均相对分子质量的变化曲线。

查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省温州市业水平考试适应性测试化学试卷(解析版) 题型:选择题
一定温度下,在密闭容器内进行某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示。则下列叙述中正确的是

A .反应的化学方程式为2Y(g)=X(g)
B. t1时,Y的浓度是X浓度的1.5倍
C .t2时,可逆反应达到化学平衡状态
D.t3时,逆反应速率大于正反应速率
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高二下学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.两种有机物具有相同的相对分子质量和不同的结构,则互为同分异构体
B.质量相同的两种有机物完全燃烧生成质量相同的水,则两有机物最简式相同
C.两种有机物结构相似具有相同的通式,则互为同系物
D.两种核素具有相同质子数,不同的质量数,则互为同位素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com