
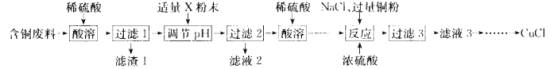
����Ŀ���Ȼ���ͭ(CuCl)�㷺Ӧ����ұ�𡢵�ơ�ҽҩ����ҵ��ijͬѧ�Ժ�ͭ����(��Ҫ�ɷ��� CuO��MgO��MnO��SiO2������������)Ϊ��Ҫԭ���Ʊ�CuCl����Ҫ�������£�
��֪����CuCl������ˮ���Ҵ� ���ڳ�ʪ�Ŀ������ױ�������
����ˮ��Һ�д���ƽ�� ��CuCl(��ɫ)+2Cl-![]() [CuCl3]2-(ɫ����Һ)��
[CuCl3]2-(ɫ����Һ)��
�����ֽ����������↑ʼ��������ȫ������pH���±���
�������� | ��ʼ������ pH | ��ȫ������ pH |
Mg(OH)2 | 8. 4 | 10. 8 |
Cu(OH)2 | 4.2 | 6. 7 |
Mn(OH)2 | 7. 8 | 8. 8 |
�ʴ��������⣺
(1)����1 ����Ҫ�ɷ��� _________________(д��ѧʽ����ͬ)��
(2)����pH�����÷�ĩ״�Լ� X ��_____________��pH�ĵ��ڷ���Ϊ____________��
(3)����Ӧ������ Cu2+ +Cu+6Cl-=2[CuCl3]2-����������ȫ��Ӧ��������_______________��
(4)������Һ3�� �Ӵ�����ˮ�����˿ɵ� CuCl�����ó����������Ҵ�ϴ�ӣ����ڵ����¸����ԭ����___________��
(5)��Ʒ���ȵIJⶨ���������£���ȡmg����������ƿ�У�����ֱ�� 4 ~ 5 mm ������������������ 10 mL FeCl3��Һ��ҡ������Ʒȫ���ܽ��(CuCl+FeCl3=CuCl2+FeCl2)���ټ���50 mL��ˮ��2���ڷ�����ָʾ����������c mol L-1 ���������[Ce(SO4)2]����Һ�ζ�(Fe2++Ce4+=Fe3++Ce3+)'�����յ�ʱ����������������ҺV mL��
����ƿ�м��벣�����������____________________��
����Ʒ�� CuCl ����������Ϊ_____(�г�����ʽ���� , �ú�(c��m��V�Ĵ���ʽ��ʾ)��
���𰸡�SiO2 CuO��Cu(OH)2��CuCO3��Cu2(OH)2CO3 6.7��pH��7.8 ��Һ����ɫ��Ϊ��ɫ CuCl�������Ҵ����Ҵ��ӷ������¸���ʱ�ɷ�ֹCuCl���� �����Լ���CuCl���ܽ� ![]() ��100%
��100%
��������
��ͭ����(��Ҫ�ɷ��� CuO��MgO��MnO��SiO2������������)����ϡ�����������ܽⲢ���й���1������SiO2����ϡ���ᷴӦ����õ�������1ΪSiO2����ҺΪ��Ҫ����Cu2+��Mg2+��Mn2+��![]() ��������Һ������Һ�м���X�Լ�������ҺpHֵ�����й���2���ɽ���Һ�е�Cu2+ת��Ϊ��������Һ�з������������Һ2��Ҫ����Mg2+��Mn2+��
��������Һ������Һ�м���X�Լ�������ҺpHֵ�����й���2���ɽ���Һ�е�Cu2+ת��Ϊ��������Һ�з������������Һ2��Ҫ����Mg2+��Mn2+��![]() �����˺�õ��ij���Cu(OH)2�������ϡ��������ܽ�õ�����Cu2+����ɫ��Һ������Һ�м���NaCl��Ũ���ἰ����ͭ�ۣ�������Ӧ��Cu2+ +Cu+6Cl-=2[CuCl3]2-��ת��Ϊ����[CuCl3]2-����ɫ��Һ���ٽ��й���3�õ�����[CuCl3]2-��Һ3������Һ3����һϵ�еIJ�����õ���Ʒ�Ȼ���ͭ(CuCl)���ݴ˷������
�����˺�õ��ij���Cu(OH)2�������ϡ��������ܽ�õ�����Cu2+����ɫ��Һ������Һ�м���NaCl��Ũ���ἰ����ͭ�ۣ�������Ӧ��Cu2+ +Cu+6Cl-=2[CuCl3]2-��ת��Ϊ����[CuCl3]2-����ɫ��Һ���ٽ��й���3�õ�����[CuCl3]2-��Һ3������Һ3����һϵ�еIJ�����õ���Ʒ�Ȼ���ͭ(CuCl)���ݴ˷������
(1)���ݷ���������1 ����Ҫ�ɷ���SiO2��
(2)����pH����Ŀ���ǽ���Һ�е�Cu2+ת��Ϊ������������Һ�з�����������÷�ĩ״�Լ� X ������Һ�е������ӷ�Ӧ�ı���Һ��pHֵ���Ҳ��γ��������������ʳ��������ĩ״�Լ� X������CuO��Cu(OH)2��CuCO3��Cu2(OH)2CO3������һ�֣�����pHֻ����Cu2+��ȫת��Ϊ������Mg2+��Mn2+��Ȼ������Һ�У����ݱ����н����������↑ʼ��������ȫ������pH���ݣ�pH�ĵ��ڷ���Ϊ6.7��pH��7.8��
(3)�����2��õ��ij���Cu(OH)2�м�ϡ��������ܽ�õ�����Cu2+����ɫ��Һ������Ӧ�����跢�� Cu2++Cu+6Cl-=2[CuCl3]2-��������֪��Ϣ��֪[CuCl3]2-��ɫ�����������ȫ��Ӧ����������Һ����ɫ��Ϊ��ɫ��
(4)������Һ3�� �Ӵ�����ˮ�����˿ɵ� CuCl�����ó����������Ҵ�ϴ�ӣ����ڵ����¸����ԭ����CuCl�������Ҵ����Ҵ��ӷ������¸���ʱ�ɷ�ֹCuCl���ʣ�
(5)����ƿ�м��벣����������ǽ����Լ���CuCl���ܽ⣻
�ڸ��ݷ�ӦCuCl+FeCl3=CuCl2+FeCl2��Fe2++Ce4+=Fe3++Ce3+�ɵã�CuCl~ Fe2+~Ce(SO4)2����n(CuCl)=n[Ce(SO4)2]=cmol L-1��V��10-3L=cV��10-3mol��m(CuCl)= cV��10-3mol��99.5g/mol=99.5��cV��10-3g������Ʒ�� CuCl ����������Ϊ![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�����2������ϩ��![]() ��������˵����ȷ����
��������˵����ȷ����
A. ����ʹϡ���������Һ��ɫ
B. ���Է����ӳɾۺϷ�Ӧ
C. ����������ԭ�ӹ�ƽ��
D. ������ˮ���ױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ݻ���ͬ�������У�һ��ʢ��NH3���壬��һ��ʢ��H2��Cl2�Ļ�����壬��ͬ��ͬѹ�£��������ڵ�����һ��������ͬ����
A.ԭ����B.������C.����D.�ܶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б�ʾ��Ӧ NaHSO4+NaHCO3=Na2SO4 + H2OʮCO2����������Ļ�ѧ���ﲻ��ȷ����
A.CO2�Ľṹʽ�� O=C= O
B.H2O�ĵ���ʽ��![]()
C.Na+�Ľṹʾ��ͼ��![]()
D.ˮ��Һ�У�NaHCO3�ĵ��뷽��ʽ�� NaHCO3=Na+ + H+ + CO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NO�ڴ���������ֽⷴӦ������ͼ��ʾ(TS��ʾ��Ӧ�еĹ���̬)�������й�˵������ȷ����
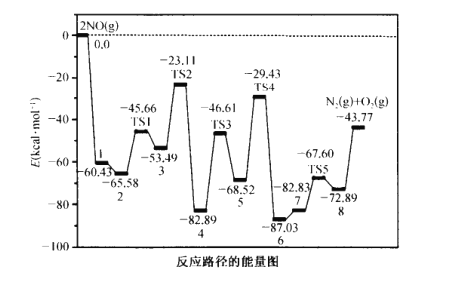
A.�ֽⷴӦ���Ȼ�ѧ����ʽΪ 2NO(g)![]() N2(g)+O2(g)��H = +43.77 kcal mol-1
N2(g)+O2(g)��H = +43.77 kcal mol-1
B.�м����3�еļ��ܴ����м����4�ģ��м����3���ȶ�
C.�����С�5��TS4��6���Ļ��������̾���������Ӧ�Ŀ���
D.ʹ�ø�Ч����������NO������������Ӷ�Ӱ�췴Ӧ�ȵĴ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���M �Ľṹ��ʽ���£������й�M ��������ȷ���ǣ� ��
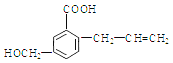
A. M�ķ���ʽΪC11H12O3
B. ��ʹ������Ȼ�̼��Һ��ɫ
C. һ�������£�M�����ɸ߷��ӻ�����
D. �ܷ����ӳɷ�Ӧ���ܷ���ȡ����Ӧ
���𰸡�D
��������
����A���������ʵĽṹ��ʽ��֪M�ķ���ʽ��C11H12O3����ȷ�� B�������ʵķ����к���̼̼˫���������ʹ������Ȼ�̼��Һ��ɫ����ȷ��C�� �����ʵķ����к���̼̼˫������һ�������·����Ӿ۷�Ӧ�γɸ߾����ȷ��D�� ������M����̼̼˫��������ܷ����ӳɷ�Ӧ�����д��ǻ����Ȼ�����˿��Է���ȡ����Ӧ������
���㣺�����л���Ľṹ�����ʵĹ�ϵ��֪ʶ��
�����͡���ѡ��
��������
22
����Ŀ�������йؽ�����ʴ�������˵������ȷ���ǣ� ��
A. ���������绯ѧ��ʴʱ��������ˮĤ�����ԣ������������ķ�ӦΪ��2H2O+O2+4eһ= 4OHһ
B. �ڳ�ʪ�Ŀ����У���ͭ��ͭп�Ͻ���Ʒ�ȴ�ͭ��Ʒ���ײ���ͭ��
C. ������Ʒ�ں�ˮ�бȵ�ˮ�и���������ʴ
D. �ӱ����Ͽ���������ʴ�ǽ���ԭ��ʧȥ���ӱ�������ӱ������Ĺ���
���𰸡�B
��������A�����������绯ѧ��ʴʱ��������ˮĤ�����Է���������ʴ�������������ķ�ӦΪ��2H2O+O2+4eһ=4OHһ��A��ȷ��B���ڳ�ʪ�Ŀ����������绯ѧ��ʴ��п�Ľ�����ǿ��ͭ����˻�ͭ��ͭп�Ͻ���Ʒ�ȴ�ͭ��Ʒ�����ײ���ͭ����B����C����ˮ�к������Ũ�ȴ�ˮ�к������Ũ��С���ʽ�����Ʒ�ں�ˮ�бȵ�ˮ�и���������ʴ��C��ȷ��D���ӱ����Ͽ���������ʴ�ǽ���ԭ��ʧȥ���ӱ�������ӱ������Ĺ�����D��ȷ����ѡB��
�����͡���ѡ��
��������
23
����Ŀ������˵������ȷ����
A. ��ѿ�Ǽ���ˮ�������ܷ���������Ӧ
B. ����ˮ���ɼ��𱽷���Һ��2,4-�Ѷ�ϩ�ͼױ�
C. �����������£�![]() ��ˮ�������
��ˮ�������![]() ��
��![]()
D. �øʰ���![]() �ͱ�����
�ͱ�����![]() ���������γ�4�ֶ���
���������γ�4�ֶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ô�����ȥ��Ӧ�Ǻϳ�ϩ���ij��÷�����ʵ���Һϳɻ���ϩ�ķ�Ӧ��ʵ��װ����ͼ��ʾ�������õ����й��������£�
��Է������� | �ܶ�(g��cm-3) | �е�/�� | �ܽ��� | |
���Ҵ� | 100 | 0.9618 | 161 | ����ˮ |
����ϩ | 82 | 0.8102 | 83 | ������ˮ |
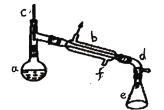
a�м���20g��������2СƬ���Ƭ����ȴ��������������1mLŨ���ᡣb��ͨ����ȴˮ��ʼ��������a�������������¶Ȳ�����90�档��Ӧ�ֲ��ﵹ��f�зֱ�������5%̼������Һ��ˮϴ�ӣ�����������ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�����ͨ������õ���������ϩ���ش��������⣺
(1)�ɻ�������ȡ����ϩ�ķ���ʽ___________________________________________��
(2)װ��b������ˮ������______(���½��ϳ����Ͻ��³�)��
(3)�������Ƭ��������______���������һ��ʱ��������ǼӴ�Ƭ��Ӧ�ò�ȡ����ȷ������______(����ȷ�𰸱��)��
A.��������B.��ȴ��C.���貹��D.��������
(4)��ʵ���������ײ����ĸ����������Ĺ���������Ϊ___________��
(5)�ڷ����ᴿ�У�ʹ�õ�������f������______�������Ȼ��ƵIJ�����_______��
(6)�ϳɹ����м���Ũ�����������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ȼ���ȵ���������ȷ����(����)
A. ��֪a g��ϩ������ȼ��ʱ����1 mol CO2��Һ̬ˮ���ų�b kJ�����������ʾ��ϩȼ���ȵ��Ȼ�ѧ����ʽΪ2C2H4(g)��6O2(g)=4CO2(g)��4H2O(l) ��H����4b kJ��mol��1
B. ���״�����ת��Ϊ�������Ȼ�ѧ����ʽ��CH3OH(g)��![]() O2(g)=CO2(g)��2H2(g) ��H����192.9 kJ��mol��1����CH3OH(g)��ȼ����Ϊ192.9 kJ��mol��1
O2(g)=CO2(g)��2H2(g) ��H����192.9 kJ��mol��1����CH3OH(g)��ȼ����Ϊ192.9 kJ��mol��1
C. H2(g)��ȼ������285.8 kJ��mol��1����2H2O(g)=2H2(g)��O2(g) ��H����571.6 kJ��mol��1
D. �����ǵ�ȼ������2800kJ��mol��1����![]() C6H12O6(s)��3O2(g)=3CO2(g)��3H2O(l) ��H����1400kJ��mol��1
C6H12O6(s)��3O2(g)=3CO2(g)��3H2O(l) ��H����1400kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
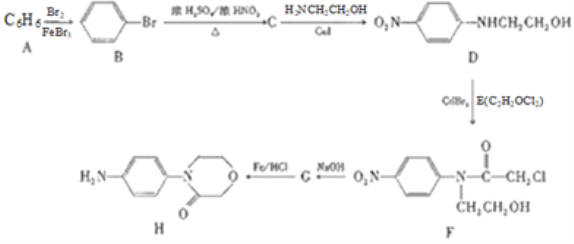
����Ŀ��H�Ǻϳ�Ԥ������Ѫ˨�γ�(![]() )��ԭ��ҩ����ɳ���м��壬��ϳ�·����ͼ��
)��ԭ��ҩ����ɳ���м��壬��ϳ�·����ͼ��
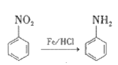
��֪��
(1)A�Ļ�ѧ����Ϊ_________________��C�к��й����ŵ�����Ϊ__________________��
(2)C��D�ķ�Ӧ����Ϊ__________________��
(3)G�Ľṹ��ʽΪ______________________��
(4)D��F�Ļ�ѧ����ʽΪ__________________________________________________��
(5)��������������D��ͬ���칹����_______________��(�����������칹)�����к˴Ź���������6����ҷ����֮��Ϊ4:2:1:1:1:1�Ľṹ��ʽΪ____________________(дһ��)��
�ٱ�������3��ȡ����������������ֱ�Ӻͱ����������ۿ��Ժ�![]() ��Һ��Ӧ����
��Һ��Ӧ����![]() �������������Ʒ�Ӧ����
�������������Ʒ�Ӧ����![]() ��
��
(6)��֪��![]() ����CΪԭ�Ϻϳ�
����CΪԭ�Ϻϳ�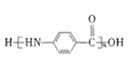 �ĺϳ�·��Ϊ____________________________________________(�����Լ���ѡ)��
�ĺϳ�·��Ϊ____________________________________________(�����Լ���ѡ)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com