
【题目】下列说法正确的是( )
A.![]() 晶体中既含有离子键,又含有共价键
晶体中既含有离子键,又含有共价键
B.![]() 晶体是原子晶体,加热融化时需克服分子间作用力和共价键
晶体是原子晶体,加热融化时需克服分子间作用力和共价键
C.HCl、HBr、HI的热稳定性依次增强
D.化学键的被破坏的过程一定都涉及化学反应
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、M的原子序数依次增大,元素X的一种高硬度单质是宝石,Y2+的电子层结构与Ne相同,Z的质子数为偶数,室温下M的单质为淡黄色固体,下列有关说法正确的是( )
A.Y单质能在X的最高价氧化物中燃烧,发生置换反应
B.X、Z、M的最简单气态氢化物的热稳定性依次增强
C.X、Y、Z、M的原子半径依次减小
D.化合物![]() 的熔点高于化合物YM的熔点
的熔点高于化合物YM的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与工农业生产和人类生活密切相关。下列说法中不正确的是( )
A.明矾[KAl(SO4)2·12H2O]可用作净水剂
B.海轮外壳上镶入锌块,可减缓船体的腐蚀
C.聚氯乙烯塑料袋可用于包装食品
D.减少化石燃料使用,有利于降低空气中PM2.5(直径2.5μm以下细颗粒物)的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色酸性溶液中能大量共存的一组离子是
A.Na+、K+、HCO3、NO3 B.NH4+、SO42、Al3+、NO3
C.Na+、Ca2+、NO3、CO32 D.K+、MnO4、NH4+、NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.NO是第一个被发现的生命体系气体信号分子,具有舒张血管的功能。工业上可用“氨催化氧化法”生产NO,主要副产物为N2。请回答下列问题:
(1)以氨气、氧气为原料,在催化剂存在下生成NO和副产物N2的热化学方程式如下:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)
4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)
2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)![]() 2NO(g) △H3③,则上述反应热效应之间的关系式为△H3 =___________________。
2NO(g) △H3③,则上述反应热效应之间的关系式为△H3 =___________________。
(2)某化学研究性学习小组模拟工业合成NO的反应。在1110K时,向一恒容密闭容器内充入1mol NH3和2.8mol O2,加入合适催化剂(催化剂的体积大小可忽略不计),保持温度不变,只发生反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H<0。
4NO(g)+6H2O(g) △H<0。
①下列各项能说明反应已达到化学平衡状态的是_______。(填字母序号)
a.5c(NH3)=4c(O2)
b.N-H键的生成速率与O-H键的生成速率相等
c.混合气体的压强不变
d.混合气体的密度不变
②若其他条件不变,将容器改为恒容的绝热容器,在达到平衡后的体系温度下的化学平衡常数为K1,则K1_____K(填“>”、“<”或“=”)。
II.(3)某化学研究性学习小组模拟用CO和H2合成甲醇,其反应为:CO(g)+2H2(g) ![]() CH3OH(g)△H<O。在容积固定为1L的密闭容器内充入2mol CO和4 mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
CH3OH(g)△H<O。在容积固定为1L的密闭容器内充入2mol CO和4 mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
则反应从开始到20min时,以CO浓度变化表示的平均反应速率v(CO)=_______,该温度下平衡常数K=_______。
III.(4)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

①B极上的电极反应式为_____________。
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到5.6 L(标准状况)气体时,消耗甲烷的体积为________L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法正确的是
A. HOCH2COOH在一定条件下可与O2、 NaHCO3溶液、乙醇、乙酸发生反应,且反应类型相同
B. C2H3COOC2H5存在C4H9COOH时可以加入饱和NaOH溶液后分液除去
C. 金刚烷(如图结构)含有属于芳香化合物的同分异构体
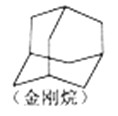
D. 与 NaHCO3溶液反应产生CO2的链状有机物C4H6O2,与HBr加成可生成5种同分异构体(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计如图所示装置(夹持装置略去),在实验室模拟侯氏制碱工艺中NaHCO3的制备。下列说法错误的是
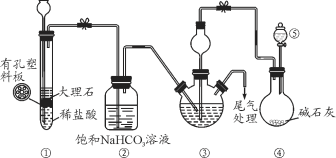
A. 装置①也可用于制取H2
B. ③、⑤中可分别盛放饱和食盐水和浓氨水
C. 应先向③中通入足量NH3,再通入足量CO2
D. ③中反应的离子方程式为NH3+CO2+H2O=NH4++HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com