
(13分)如图所示3套实验装置,分别回答下列问题。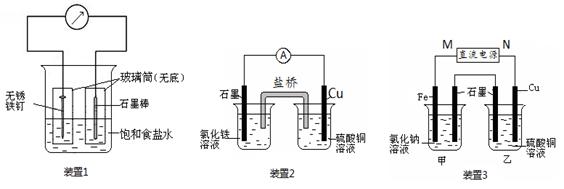
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6] 溶液,即可观察到铁钉附近的溶液有蓝色沉淀,表明铁被 (填“ 氧化”或“还原”); 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。
① 电源的M端为 极(填“正”或“负”),甲烧杯中铁电极的电极反应为 。
② 乙烧杯中电解反应的化学方程式为 。
③ 停止电解,取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g,甲烧杯中产生的气体标准状况下体积为 mL 。
(13分)(1)氧化(1分); O2+ 4e-+ 2H2O = 4OH-(2分)
(2)正(1分), 2Fe3+ + Cu = 2Fe2+ + Cu2+ (2分)
(3)① 正(1分), Fe -2e-= Fe2+(2分)
② 2CuSO4+ 2H2O 2Cu + O2↑ + 2H2SO4 (2分) ③ 224 (2分)
2Cu + O2↑ + 2H2SO4 (2分) ③ 224 (2分)
解析试题分析:(1)装置1为铁的电化学腐蚀,铁钉附近的溶液有蓝色沉淀,表明铁被氧化,铁为负极,碳为正极。观察到碳棒附近的溶液变红,说明在碳极上氧气得电子生成OH-离子,反应的电极反应式为O2+ 4e-+ 2H2O = 4OH-。
(2)装置2为原电池,负极为Cu,铜失去电子,生成铜离子而溶解。石墨是正极,溶液中的铁离子得到电子生成亚铁离子,所以总的离子方程式是2Fe3+ + Cu = 2Fe2+ + Cu2+。
(3)①反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,说明在石墨电极上生成OH-离子,即石墨是阴极,所以铁是阳极,M是电源的正极,则铁电极的方程式是Fe -2e-= Fe2+。
②乙烧杯电解硫酸铜溶液,石墨为阳极,铜是阴极,所以电解的总方程式是2CuSO4+2H2O 2Cu + O2↑+ 2H2SO4。
2Cu + O2↑+ 2H2SO4。
③取出Cu电极,洗涤、干燥、称量、电极增重0.64g,则生成Cu的物质的量为0.64g ÷64g/mol =0.01mol,转移的电子的物质的量为0.01mol×2=0.02mol
根据甲烧杯产生气体的电极反应可知
2H++2e-=H2↑
2mol 22.4L
0.02mol V
所以V=0.224L。
考点:考查电化学原理的综合应用、金属的腐蚀和防护、电极反应式的书写、电极名称的判断以及有关计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,难易适中,侧重考查学生分析问题、解决问题的能力。做题时要注意电极的判断和电极反应的书写,注意串联电路中各电极转移的电子数目相等,利用反应的方程式计算即可。


科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)如图所示3套实验装置,分别回答下列问题:
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0、2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0、5 mol/L的CuSO4溶液。反应一段时间后,停止通电。取出Cu电极,洗涤、干燥、称量、电极增重 0、64 g。
① 电源的M端为 极,甲烧杯中铁电极的电极反应为 ;
② 乙烧杯中电解反应的离子方程式为 ;
③ 甲、乙两烧杯中生成的气体标准状况下共 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)如图所示3套实验装置,分别回答下列问题:
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g。
① 电源的M端为 极,甲烧杯中铁电极的电极反应为 ;
② 乙烧杯中电解反应的离子方程式为 ;
③ 甲、乙两烧杯中生成的气体标准状况下共 mL。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省南安市侨光中学高二上学期期末考试化学试卷 题型:实验题
如图所示3套实验装置,分别回答下列问题。
(1)装置1为铁的吸氧腐蚀实验。一段时间后,溶液略显浅绿色,表明铁被 (填“氧化”或“还原”);向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程为 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为 极;甲烧杯中铁电极的电极反应为 。
②乙烧杯中电解反应的离子方程式为 。
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为 mL。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽省高三第四次月考化学试卷 题型:填空题
(12分)如图所示3套实验装置,分别回答下列问题:
 (1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为
。
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为
。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0、2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0、5 mol/L的CuSO4溶液。反应一段时间后,停止通电。取出Cu电极,洗涤、干燥、称量、电极增重 0、64 g。
① 电源的M端为 极,甲烧杯中铁电极的电极反应为 ;
② 乙烧杯中电解反应的离子方程式为 ;
③ 甲、乙两烧杯中生成的气体标准状况下共 mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com