
【题目】Ⅰ. 埃及人泽维尔用激光闪烁照相机拍摄到化学反应中化学键断裂和形成的过程,因而获得1999年诺贝尔化学奖。激光有很多用途,例如波长为10.3 微米的红外激光能切断B(CH3)3分子中的一个B-C键,使之与HBr发生取代反应:B(CH3)3+HBr![]() B(CH3)2Br+CH4
B(CH3)2Br+CH4
而利用9.6微米的红外激光却能切断两个B-C键,并与HBr发生二元取代反应。
(1)试写出B(CH3)3与HBr二元取代的化学方程式:___________________
(2)利用5.6 g B(CH3)3和9.72 g HBr正好完全反应,则生成物中甲烷的物质的量为____。其他两种产物的物质的量之比为___________。
Ⅱ.橡胶可用于制造汽车内胎,合成丁基橡胶的一种单体A的分子式为C4H8,A氢化后得到2甲基丙烷。完成下列填空:
(1)A可以聚合,写出A的两种聚合方式(以化学方程式表示):____________________。
(2)A与某烷发生反应生成分子式为C8H18的物质B,B的一卤代物只有4种,且碳链不对称。写出B的结构简式_______________。
(3)写出将A通入下列两种溶液后出现的现象。
A通入溴水:______________;A通入溴的四氯化碳溶液:________________。
【答案】 ![]() 0.12mol
0.12mol ![]()
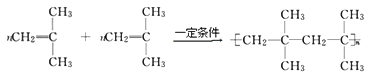 ;
;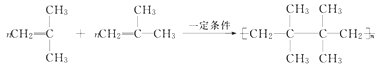
 红棕色褪去且溶液分层 红棕色褪去
红棕色褪去且溶液分层 红棕色褪去
【解析】(1)由反应信息可知,B(CH3)3分子中的一个B-C键断裂,Br原子取代甲基,甲基与H原子结合生成甲烷,B(CH3)3和HBr反应生成其二溴代物为B(CH3)Br2,1molB(CH3)3发生二溴取代同时生成2mol甲烷,反应方程式为:B(CH3)Br2+2HBr![]() B(CH3)Br2+2CH4;
B(CH3)Br2+2CH4;
(2)5.6gB(CH3)3的物质的量为![]() =0.1mol,9.72gHBr的物质的量为
=0.1mol,9.72gHBr的物质的量为![]() =0.12mol,假设生成的B(CH3)2Br为xmol,生成B(CH3)Br2为ymol,根据B原子及溴原子守恒,则:x+y=0.1、x+2y=0.12;解得:x=0.08,y=0.02,
=0.12mol,假设生成的B(CH3)2Br为xmol,生成B(CH3)Br2为ymol,根据B原子及溴原子守恒,则:x+y=0.1、x+2y=0.12;解得:x=0.08,y=0.02,
故B(CH3)2Br与B(CH3)Br2的物质的量之比为:0.08mol:0.02mol=4:1,
由碳原子守恒可知,甲烷的物质的量=0.1mol×3-0.08mol×2-0.02mol=0.12mol;
Ⅱ.(1)A氢化后得到2-甲基丙烷,可知A为2-甲基-1-丙烯,他发生加聚反应的方式有两种: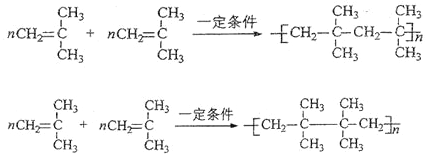 ;
;
(2)C8H18的各种同分异构体中,一卤代物只有4种,且碳链不对称的结构简式仅有一个,为: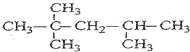 ;
;
(3)A通入溴水,则A与溴水发生加成反应得到卤代烃,卤代烃和水互不相溶,故红棕色褪去且溶液分层;A通入溴的四氯化碳溶液时,则A与溴水发生加成反应得到卤代烃,卤代烃和四氯化碳相溶,故只看到红棕色褪去。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案科目:高中化学 来源: 题型:
【题目】下列描述中正确的是
A. CS2为V形的极性分子 B. ClO3-的空间构型为平面三角形
C. SF6中的空间构型为正四面体形 D. SiF4和SO32-的中心原子均为sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1 nm~100 nm的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质:①是溶液;②是胶体;③能产生丁达尔效应;④能透过滤纸;⑤不能透过滤纸;⑥静置后,会析出黑色沉淀。下列组合中的说法全部正确的是
A.①④⑥ B.②③④ C.②③⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种有机物组成的混合物,当混合物总质量一定时,无论A、B以何种比例混合,完全燃烧后,生成CO2的质量为定值,则符合这一条件的有机物组合是( )
A. 甲醇(CH3OH)和乙二醇(HOCH2CH2OH) B. 甲醛(HCHO)和乙醛 (CH3CHO)
C. CH4和 D. 苯(C6H6)和苯酚(C6H5OH)
D. 苯(C6H6)和苯酚(C6H5OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2016天津)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是_________(至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:____________。
(2)氢气可用于制备H2O2。已知:
H2(g)+A(l)=B(l) ΔH1
O2(g)+B(l)=A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH____0(填“>”、“<”或“=”)。
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)![]() MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
a.容器内气体压强保持不变
b.吸收y mol H2只需1 mol MHx
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH![]() FeO42+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
FeO42+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。

①电解一段时间后,c(OH)降低的区域在_______(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______。
③c( Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置,下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铁片上发生的反应为:Fe-2e-=Fe2+
C. a和b用导线连接时,电子从Cu片流向铁片
D. a和b用导线连接时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是( )
A.冬季烧煤炭供热取暖与雾霾的形成无必然联系
B.食品包装袋中充人氮气可防腐
C.钢铁表面镀锌可防止铁的腐蚀
D.回收地沟油制造生物柴油符合环境保护的要求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时,将nmol/L氨水滴入10mL1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是

A. a点Kw=1.0×10-14
B. 水的电离程度:c>b>a>d
C. b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D. 25℃时,氨水的电离平衡常数K=10-7/(10n-1)mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com