
【题目】将一定量的CO2气体通入2LNaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl物质的量关系如图所示,下列说法不正确的是

A. O点溶液中所含溶质的化学式为NaOH、Na2CO3
B. a点溶液中c(HCO3-)>c(CO32-)
C. 标准状况下,通入CO2的体积为44.8L
D. 原NaOH溶液的物质的量浓度为5mol/L
【答案】D
【解析】
A.Na2CO3跟盐酸的反应是分步进行的:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,HCl与Na2CO3、NaHCO3都按1:1反应,由图象可知生成二氧化碳消耗的HCl的物质的量小于从反应到开始产生二氧化碳阶段消耗的HCl,故溶液中溶质为NaOH、Na2CO3,故A说法正确;
B.根据A分析可知,0到a点发生反应为:氢离子与氢氧根离子反应生成水,氢离子与碳酸根反应生成碳酸氢根,发生的离子反应为:H++OH-=H2O、CO32-+H+=HCO3-,则在a点时溶质主要是NaCl和NaHCO3,溶液中c(HCO3-)>c(CO32-),故B说法正确;
C.由图可知,a点时开始生成气体,故发生反应为:NaHCO3+HCl=NaCl+H2O+CO2↑,至生成二氧化碳体积最大时,该阶段消耗的HCl的物质的量为2mol,由方程式可知产生二氧化碳的物质的量为2mol,生成的二氧化碳的物质的量等于开始通入的二氧化碳的物质的量,故开始通入的二氧化碳的体积为2mol×22.4L/mol=44.8L,故C说法正确;
D.加入5molNaCl生成二氧化碳体积最大,此时溶液中溶质为NaCl,根据氯离子守恒有n(NaCl)=n(HCl),根据钠离子守恒有n(NaOH)=n(NaCl),故n(NaOH)=n(HCl)=5mol,所以c(NaOH)=![]() =2.5mol/L,故D说法错误;
=2.5mol/L,故D说法错误;
答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,向容积可变的密闭容器中通入 N2 和 H2,发生反应:N2(g) + 3H2(g) ![]() 2NH3(g) ΔH<0 达到平衡后,试回答下列问题:
2NH3(g) ΔH<0 达到平衡后,试回答下列问题:
(1)该条件下,反应的平衡常数表达式K=__________,若降低温度,K 值将______(填“增大”、“减小” 或“不变”)。 达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将_______(填“向逆反应方向”、“向正反应方向”或“不”)移动,平衡常数_____(填“增大”、“减小” 或“不变”)。
(2)下列能说明该反应已达到平衡状态的有(_____)
A.容器内压强不随时间变化而变化
B.混合气体总分子数不随时间变化而变化
C.混合气体的颜色不再改变
D.c(N2)与c(H2)的比值为1:3
E.容器中气体的密度不再改变
(3)既加快反应速率又使平衡右移的方法是(_____)
A.降低温度 B.加入正催化剂 C.减小容器体积 D.再通入和原来相等量的 N2 和 H2
(4)在A、B 两个容积相同的容器中各充入 1mol N2 和 3mol H2,A 容器保持恒温恒容达到平衡时氢气的物质的量为x,B 容器保持恒温恒压达到平衡时氢气的物质的量为y,则 x________y(“>”“<”或“=”)。
(5)在容积为2.0 L且体积不变的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为![]() ,则该条件下N2的平衡转化率为__________。
,则该条件下N2的平衡转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 碘晶体受热转变为碘蒸气,吸收的热量用于断裂共价键
B. 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
C. 多电子原子中,在离核较近的区域内运动的电子能量较高
D. 两个非金属元素原子间只可能形成共价键,而含金属元素的化合物中一定含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验探究:探究碳、硅元素的非金属性的相对强弱.根据要求完成下列各小题.
(1)实验装置:

填写所示仪器名称B:______
(2)实验步骤:
连接仪器、_______、加药品后,打开a、然后滴入浓硫酸,加热.
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是____;装置E中酸性KMnO4溶液的作用是________ ;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是__________;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性_____(填“能”或“否”),试管D中发生反应的离子方程式是_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁烷与异丁烷互为同分异构体的依据是
A.具有相似的物理性质
B.具有相似的化学性质
C.具有不同的分子结构
D.分子式相同,但分子内碳原子的连接方式不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图的转化关系判断下列说法正确的是(反应条件已略去)( )
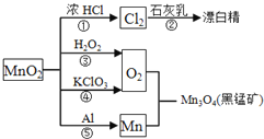
A. 反应①②③④⑤均属于氧化反应和离子反应
B. 反应⑤说明该条件下铝的还原性强于锰
C. 相同条件下生成等量的O2,反应③和④转移的电子数之比为1︰1
D. 反应①中氧化剂与还原剂的物质的量之比为1︰4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com