



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� ��� |
KClO3��g�� | ������ | �������壨mL�� ��������Ϊ����� |
��ʱ��s�� | ��ѧʽ | ������g�� | ʵ�ʻ��� | 1 | 0.6 | - | - | - | 10 | 480 | 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 | 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 | 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 | 5 | 0.6 | Cr2O3 | 0.20 | �쳣 | 67.2 | 188.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� ��� |
KClO3 ��g�� |
������ | �������壨mL�� ��������Ϊ����� |
��ʱ��s�� | ||
| ��ѧʽ | ������g�� | ���� | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | �쳣 | 67.2 | 188.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�긣��ʡ�ϰ�һ�и߶���ѧ�����п��Ի�ѧ�������Ծ� ���ͣ�ʵ����
(9��)ijͬѧ�Ե������ڹ���Ԫ�ز���Ũ�����Ȥ����̽���Ƿ�ֻ��MnO2�ܴ�KClO3���ȷֽ�?CuO��Fe2O3��Cr2O3�ȶ�����ص����ȷֽ���û�д�����?���д����ã�Ч������?��������һ�����ʵ��̽����
I���������ƣ�_________________________��
��ʵ����������
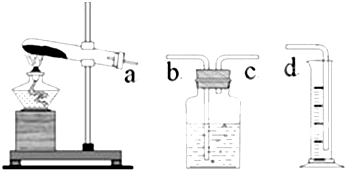
ʵ���Լ����������̡�������������ͭ���������������
��ʵ�鲽�裺��
����ʵ�����ݣ�
| ʵ�� ��� | KClO3 (g) | ������ | ��������(mL) (������Ϊ���) | ��ʱ(s) | ||
| ��ѧʽ | ����(g) | ���� | ||||
| 1 | 0.6 | �� | �� | �� | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | �쳣 | 67.2 | 188.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�츣��ʡ�߶���ѧ�����п��Ի�ѧ�������Ծ� ���ͣ�ʵ����
(9��)ijͬѧ�Ե������ڹ���Ԫ�ز���Ũ�����Ȥ����̽���Ƿ�ֻ��MnO2�ܴ�KClO3���ȷֽ�?CuO��Fe2O3��Cr2O3�ȶ�����ص����ȷֽ���û�д�����?���д����ã�Ч������?��������һ�����ʵ��̽����
I���������ƣ�_________________________��
��ʵ����������
ʵ���Լ����������̡�������������ͭ���������������
��ʵ�鲽�裺��
����ʵ�����ݣ�
|
ʵ�� ��� |
KClO3 (g) |
������ |
��������(mL) (���������) |
��ʱ(s) |
||
|
��ѧʽ |
����(g) |
���� |
||||
|
1 |
0.6 |
�� |
�� |
�� |
10 |
480 |
|
2 |
0.6 |
MnO2 |
0.20 |
90% |
67.2 |
36.5 |
|
3 |
0.6 |
CuO |
0.20 |
90% |
67.2 |
79.5 |
|
4 |
0.6 |
Fe2O3 |
0.20 |
90% |
67.2 |
34.7 |
|
5 |
0.6 |
Cr2O3 |
0.20 |
�쳣 |
67.2 |
188.3 |
V��ʵ�����ۣ�
�����ñ��3��ʵ���������KClO3�ķֽ��ʣ�Ϊ______��(����һλС��)��
������Cr2O3��ʵ��ʱ���д̼�����ζ�����������ͬʱ��ɫ�Ļ�������ٻ�ɫ��K2Cr2O7�����ô̼������������______���ѧʽ)���� ���顣������ţ�
A��ʪ�����ɫʯ����ֽ B��ʪ��ĵ⻯�ص�����ֽ
C��ʪ���PH��ֽ D��ʪ��ĺ�ɫʯ����ֽ
����ʵ����ۣ�________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�긣��ʡȪ�����ϰ�һ�и�һ���ϣ����л�ѧ�Ծ��������棩 ���ͣ������
| ʵ�� ��� | KClO3 ��g�� | ������ | �������壨mL�� ��������Ϊ����� | ��ʱ��s�� | ||
| ��ѧʽ | ������g�� | ���� | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | �쳣 | 67.2 | 188.3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com