
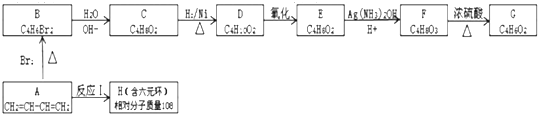

 ,由反应信息①,结合相对分子质量可知2分子CH2=CH-CH=CH2发生加成反应生成六元环化合物H为
,由反应信息①,结合相对分子质量可知2分子CH2=CH-CH=CH2发生加成反应生成六元环化合物H为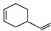 ,据此解答.
,据此解答. ,由反应信息①,结合相对分子质量可知2分子CH2=CH-CH=CH2发生加成反应生成六元环化合物H为
,由反应信息①,结合相对分子质量可知2分子CH2=CH-CH=CH2发生加成反应生成六元环化合物H为 ,
,| △ |
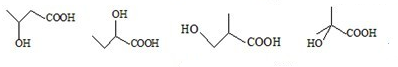 ,共有4种,
,共有4种,| △ |
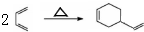 ,故答案为:
,故答案为: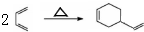 ;
; ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
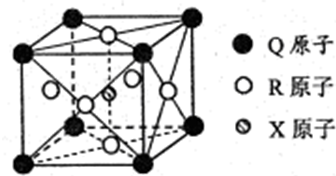
查看答案和解析>>
科目:高中化学 来源: 题型:
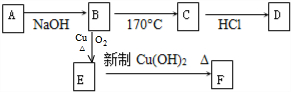
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定前 | 第一次 终点 | 第二次 终点 | 第三次 终点 | |
| 碱式滴定管 液面刻度 | 0.10mL | 19.12mL | 18.15mL | 19.08mL |

查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、M、D、E是原子序数依次增大的五种短周期元素.A元素的一种原子中不含中子.B、M、D、E分别在下表(周期表的一部分)不同的空格内占有相应的位置,E的原子序数是D的原子序数的2倍.试回答:
A、B、M、D、E是原子序数依次增大的五种短周期元素.A元素的一种原子中不含中子.B、M、D、E分别在下表(周期表的一部分)不同的空格内占有相应的位置,E的原子序数是D的原子序数的2倍.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| C |
| D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al2O3熔点很高,可用于制作耐高温材料 |
| B、硅具有半导体性能,可以制成光电池 |
| C、次氯酸钠具有强氧化性,可用于配制消毒液 |
| D、明矾水解产生具有吸附性的胶体粒子,可作漂白剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com