
分析 (1)醋酸与双氧水反应生成过氧乙酸和水,H2O2+CH3COOH$\stackrel{浓硫酸}{→}$(过氧乙酸)+H2O,结合化学方程式定量关系计算过氧化氢的质量;
(2)①加入过量KI溶液前,需除去H2O2的原因是过氧化氢也会氧化碘离子,会干扰测定结果;
②n(S2O32-)=0.01000mol/L×0.02500L=2.5×10-4mol,
CH3COOOH+2I-+2H+═I2+CH3COOH+H2O
2S2O32-+I2═2I-+S4O62-
CH3COOOH~I2~2S2O32-,
n(CH3COOOH)=$\frac{1}{2}$n(S2O32-)=$\frac{1}{2}$×2.5×10-4mol=1.25×10-4mol,
计算得到过氧乙酸样液中过氧乙酸的质量分数;
③实验过程中高锰酸钾溶液、空气中氧气都会氧化碘离子造成测定的含量偏高;
解答 解:(1)制备20g38%过氧乙酸溶液至少需要42.5%过氧化氢溶液质量为x,
H2O2+CH3COOH$\stackrel{浓硫酸}{→}$CH3COOOH+H2O
34 76
x×42.5% 20g×38%
x=8g,
故答案为:8g;
(2)①加入过量KI溶液前,需除去H2O2的原因是过氧化氢也会氧化碘离子,会干扰测定结果,反应的离子方程式为:2I-+H2O2+H+=I2+2H2O,
故答案为:2I-+H2O2+H+=I2+2H2O;
②n(S2O32-)=0.01000mol/L×0.02500L=2.5×10-4mol,
CH3COOOH+2I-+2H+═I2+CH3COOH+H2O
2S2O32-+I2═2I-+S4O62-
CH3COOOH~I2~2S2O32-,
n(CH3COOOH)=$\frac{1}{2}$n(S2O32-)=$\frac{1}{2}$×2.5×10-4mol=1.25×10-4mol,
w%=$\frac{1.25×1{0}^{-4}mol×76g/mol}{0l5000g}×\frac{100ml}{5.0ml}$×100%=38.0%,
答:n(S2O32-)=0.01000mol/L×0.02500L=2.5×10-4mol,
CH3COOOH+2I-+2H+═I2+CH3COOH+H2O
2S2O32-+I2═2I-+S4O62-
CH3COOOH~I2~2S2O32-,
n(CH3COOOH)=$\frac{1}{2}$n(S2O32-)=$\frac{1}{2}$×2.5×10-4mol=1.25×10-4mol,
w%=$\frac{1.25×1{0}^{-4}mol×76g/mol}{0l5000g}×\frac{100ml}{5.0ml}$×100%=38.0%;
③取5.00mL上述溶液与100mL碘量瓶中,再加入5.0mL2mol•L-1H2SO4溶液,用0.01mol•L-1KMnO4溶液滴定至溶液出现浅红色(以除去过氧乙酸试样中剩余H2O2),过量的高锰酸钾溶液会氧化碘离子生成碘单质导致过氧乙酸含量偏高,或空气中氧气也可以氧化碘离子为碘单质,也可以导致测定结果偏高,
故答案为:过量的KMnO4氧化I-生成I2或在酸性溶液中I-会被空气中氧气氧化为I2;
点评 本题考查了化学方程式的定量计算、氧化还原反应过程分析、滴定实验和定量计算的分析判断,主要是原理理解应用和定量计算关系,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 元素编号 | a | b | c | d | e | f | g |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -2 | +3 | +1 | +1 |
| A. | 氢化物稳定性的强弱:b>d | |
| B. | 金属性的强弱:f<g | |
| C. | 元素e的氧化物只能与酸反应 | |
| D. | 最高价氧化物对应的水化物的碱性:e<g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2 Ba2++4OH-=AlO2-+2BaSO4↓+2H2O | |
| B. | 向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O | |
| C. | 向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH4++OH-=NH3•H2O | |
| D. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在偏铝酸钠溶液中滴入少量的碳酸氢钠溶液HCO3-+AlO2-+H2O=Al(OH)3↓+CO2↑ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+离子刚好完全沉淀2Al3++6OH-+3Ba2++3SO42-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 在碳酸氢镁溶液中逐滴加入澄清石灰水至过量Ca2++Mg2++2HCO3-+2OH-=CaCO3↓+2H2O+MgCO3↓ | |
| D. | 氢氧化铁固体溶于氢碘酸 Fe(OH)3+3H+=Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
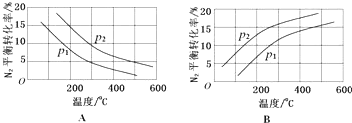
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 方案 |
| A | 除去乙酸乙酯中的乙酸 | 用NaOH溶液洗涤,分液,然后干燥 |
| B | 制备少量漂白粉 | Cl2通人澄清石灰水中,然后蒸发结晶 |
| C | 检验食盐中是否添加KIO3 | 食盐溶解,然后加入淀粉溶液 |
| D | 测定醋酸溶液浓度 | 酚酞作指示剂,用标准NaOH溶液滴定 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
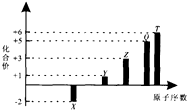
| A. | 1 mol TX2与足量X2反应生成TX3的分子数目为NA | |
| B. | Z元素形成的可溶性盐溶液可能显碱性 | |
| C. | 1 mol Y2X2与足量H2O反应转移的电子数目为2NA | |
| D. | 0.1 molQ元素的含氧酸在水中电离出的H十数目为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com