
【题目】以下叙述正确的是
A.固体氯化钠不导电,所以氯化钠是非电解质
B.铜丝能导电,所以铜是电解质
C.硫酸溶液能导电,所以H2SO4是电解质
D.三氧化硫溶于水能导电,所以三氧化硫是电解质
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】过滤后的食盐水中仍然含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2溶液;④滴入稀盐酸至无气泡产生;⑤过滤正确的操作顺序为
A.③②①⑤④
B.①②③⑤④
C.②③①④⑤
D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产生活中应用广泛,请解决下列问题。
(1)化合物甲(由氮和另一种常见的主族元素组成)是一种新型无机材料。将 8.2g 甲溶于足量的氢氧化钠溶液,可产生标准状况下为 4.48L 的气体,该气体可作制冷剂。向反应后的溶滚中逐滴加入稀盐酸,产生白色沉淀质量最大为 15.6g,继续滴加沉淀消失。则甲溶于氢氧化钠的化学方程式为_____________________。
(2)NH3催化还原氮氧化物是目前应用广泛的烟气氮氧化物脱除技术。例如:
4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) △H1
5N2(g)+6H2O(g) △H1
己知:①H2O(l)=H2O(g) △H2
②4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H3
则 NH3(g)的标准燃烧热△H=____________________。
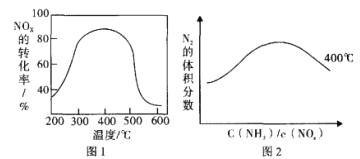
(3)以FeSO4作催化剂在不同温度下,经过相同的时间测试氨还原氮氧化物效果如图1,当反应在400~450℃,NOx 的转化率随温度升高而降低。当体系温度升至 500℃以上时. NOx 的转化率迅速下降,其可能原因是______________________。图2反映的是在400℃N2的体积分数与反应物中 c(NH3)/c(NOx)的关系,请在下面的图2上画出450℃的变化趋势曲线。
(4)N2O5 是绿色硝化试剂,溶于水可得硝酸。下图是以 N2O4为原料电解制备N2O5的装置示意图。写出阳极区生成 N2O5 的电极反应式是________________。

(5)常温下,向 0.1mol/L 氨水中加入少许 N2O5,使溶液中 c(NH3·H2O):c(NH4+)=5:9,此时溶液的 pH=___________。( 25℃时. NH3·H2O 的电离平衡常数 Kb=1.8×10-5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法或操作中,正确的有( )
①标准状况下,1 mol溴单质的体积约为22.4 L ②用托盘天平称量50.56 g KCl固体 ③用酒精从饱和碘水中萃取碘
④让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路” ⑤从含有少量氯化钠的硝酸钾溶液中提取硝酸钾可用结晶的方法
A. 1个 B. 2个
C. 3个 D. 4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Na+、K+、Cu2+ |
阴离子 | SO42-、OH- |
在下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16g。常温下各烧杯中溶液的pH与电解时间t的关系如图。据此回答下列问题:
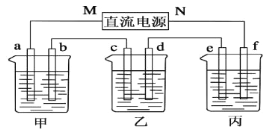
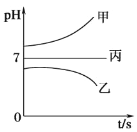
(1)M为电源的_______________极(填“正”或“负”),电极b上发生的电极反应为_____________。
(2)电极e上生成的气体在标准状态下的体积为________。
(3)写出乙烧杯中的电解池反应___________________。
(4)若电解过程中,乙烧杯中的B溶液中的金属离子全部析出,此时电解还能继续进行,原因是________________。
(5)若经过一段时间后,测得乙烧杯中c电极质量增加了16g,要使丙烧杯中的C溶液恢复到原来的状态,正确的操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
A.2v(NH3)=v(CO2)
B.密闭容器中c(NH3)∶c(CO2)=2∶1
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如图所示.已知:碳酸不能溶解Al(OH)3沉淀.
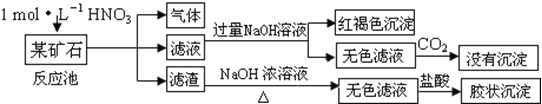
(1)Si在周期表中的位置是 .
(2)下列说法正确的是 .
a.酸性:H2CO3>H2SiO3b.原子半径:O<C<Si<Al
c.稳定性:H2O>CH4>SiH4d.离子半径:O2﹣<Al3+
(3)该矿石的组成是 ,滤渣和NaOH溶液反应的离子方程式是 .
(4)该矿石和1mol/LHNO3反应的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com