
【题目】某新型有机酰胺化合物M在工业生产中有重要的作用,其合成路线如下:

已知:①A是烃的含氧衍生物,相对分子质量为58,碳和氢的质量分数之和为44.8%,核磁共振氢谱显示为一组峰,可发生银镜反应。
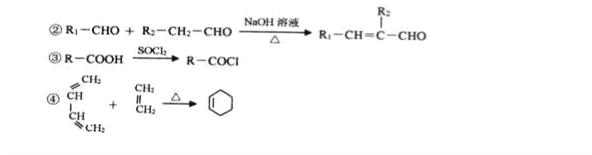
回答下列问题;
(1)E的结构简式为________________,G的名称为_____________。
(2)B中含有官能团的名称为__________________
(3)C→D的反应类型为_____________。
(4)写出B→C的化学反应方程式____________________________.F+H→M的化学反应方程式____________________________
(5)芳香族化合物W有三个取代基,是C的同分异构体,能与FeCl3溶液发生显色反应。0.5molW可与足量的Na反应生成1gH2,且核磁共振氢谱显示为五组峰,符号以上条件的W的同分异构体共有__________种,写出其中一种的结构简式______________。
(7)参照上述合成路线,以C2H4和HOCH2CH2OH为原料(无机试剂任选),设计制备OHC-CH=CH-CHO的合成路线______。
【答案】 ![]() 硝基苯 碳碳双键 醛基 加成反应(或还原反应) OHCCH=CH—CH=CHCHO+CH=CH
硝基苯 碳碳双键 醛基 加成反应(或还原反应) OHCCH=CH—CH=CHCHO+CH=CH ![]()
![]()
 2
2 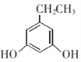 或
或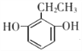
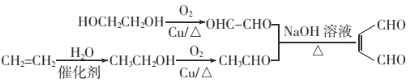
【解析】分析:A是烃的含氧衍生物,相对分子质量为58,碳和氢的质量分数之和为44.8%,则氧元素的质量分数为55.2%,A分子中的O原子数为![]() 、C原子数为
、C原子数为![]() (余数为2),故A的分子式为C2H2O2,A核磁共振氢谱显示为一组峰,可发生银镜反应,则A为乙二醛;由信息②可知,A与乙醛反应生成B,B为OHCCH=CH—CH=CHCHO;由信息④可知,B与乙烯发生加成反应生成C,则C为
(余数为2),故A的分子式为C2H2O2,A核磁共振氢谱显示为一组峰,可发生银镜反应,则A为乙二醛;由信息②可知,A与乙醛反应生成B,B为OHCCH=CH—CH=CHCHO;由信息④可知,B与乙烯发生加成反应生成C,则C为![]() ; C与氢气发生加成反应生成D,D发生氧化反应生成E,则E为
; C与氢气发生加成反应生成D,D发生氧化反应生成E,则E为![]() ;由信息③可知,E与二氯氧硫反应生成F,F为
;由信息③可知,E与二氯氧硫反应生成F,F为![]() ;苯发生硝化反应生成G,由M的结构可知,G为硝基苯;G发生还原反应生成H,则H为苯胺;F与H发生取代反应生成M。
;苯发生硝化反应生成G,由M的结构可知,G为硝基苯;G发生还原反应生成H,则H为苯胺;F与H发生取代反应生成M。
详解:(1)E的结构简式为![]() ,G的名称为硝基苯。
,G的名称为硝基苯。
(2)B中含有官能团的名称为碳碳加成反应(或还原反应)双键和醛基。
(3)C→D的反应类型为加成反应(或还原反应)。
(4)B→C的化学反应方程式为OHCCH=CH—CH=CHCHO+CH=CH ![]()
![]() ;F+H→M的化学反应方程式为
;F+H→M的化学反应方程式为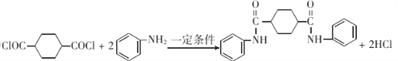 。
。
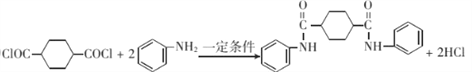
(5)芳香族化合物W有三个取代基,是C(![]() ,不饱和度等于4)的同分异构体,能与FeCl3溶液发生显色反应,则W分子中有酚羟基、三个取代基均为饱和的;0.5molW可与足量的Na反应生成1gH2,则W分子中有2个羟基;其核磁共振氢谱显示为五组峰。符合以上条件的W的同分异构体有
,不饱和度等于4)的同分异构体,能与FeCl3溶液发生显色反应,则W分子中有酚羟基、三个取代基均为饱和的;0.5molW可与足量的Na反应生成1gH2,则W分子中有2个羟基;其核磁共振氢谱显示为五组峰。符合以上条件的W的同分异构体有 和
和 ,共有2种。
,共有2种。
(7)参照上述合成路线,以C2H4和HOCH/span>2CH2OH为原料制备OHC-CH=CH-CHO,首先把乙二醇催化氧化为乙二醛;再把乙烯与水发生加成反应制备乙醇;接着,乙醇通过催化氧化制备乙醛;最后,乙二醛与乙醛通过信息②的反应合成产品。具体合成路线如下: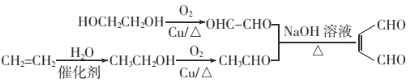 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列电离方程式错误的是( )
A.NaHCO3═Na++H++CO32﹣
B.NaHSO4═Na++H++SO42﹣
C.Mg(NO3)2═Mg2++2NO3﹣
D.Na2SO4═2Na++SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、M 均为短周期元素。25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol/L)溶液的pH和原子半径的关系如图所示。下列说法不正确的是
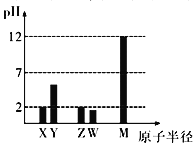
A. X、M 简单离子半径大小顺序:X>M
B. X、Y、Z、W、M 五种元素中只有一种是金属元素
C. Z 的最高价氧化物的化学式为ZO3
D. X、Z的最简单气态氢化物反应有白烟生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法正确的是
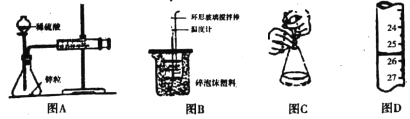
A. 图A中测定锌粒与1mol/L稀硫酸的反应速率,只需测定注射器中收集氢气的体积
B. 图B装置中进行50mL0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液发生中和反应放出热量的测定,使温度计温度升高的热量就是中和反应生成1mol水的热量
C. 图C酸碱中和滴定中,可以在滴定过程中用少量水冲洗锥形瓶内壁
D. 图D滴定管中液面位置如图所示,则此时的读数为26.50mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。
主反应:C4H10(g,正丁烷)![]() C2H4(g)+C2H6(g) △H1
C2H4(g)+C2H6(g) △H1
副反应:C4H10 (g,正丁烷)![]() CH4(g)+C3H6(g) △H2
CH4(g)+C3H6(g) △H2
回答下列问题:
(1)化学上,将稳定单质的能量定为0,生成稳定化合物时释放或吸收的能量叫做生成热,生成热可表示该物质相对能量。下表为25℃、101kPa下几种有机物的生成热:
物质 | 曱烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
生成热/kJ·mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
①书写热化学方程式时,要标明“同分异构体名称”,其理由是_______________________。
②上述反应中,△H1=______kJ/mol。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。
①下列情况表明该反应达到平衡状态的是_______(填代号)。
A.气体密度保持不变 B.[c(C2H4)·c(C2H6)]/ c(C4H10)保持不变
C.反应热不变 D.正丁烷分解速率和乙烷消耗速率相等
②为了同时提高反应速率和转化率,可采用的措施是________________。
(3)向密闭容器中充入丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,随若温度升高,乙烯产率降低,可能的原因是__________(填代号)。
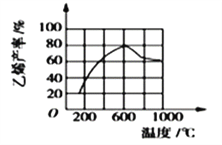
A.平衡常数降低 B.活化能降低
C.催化剂活性降低 D.副产物增多
(4)在一定温度下向1L恒容密闭容器中充入2mol正丁烷,反应生成乙烯和乙烷,经过10min达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10min内乙烯的生成速率v(C2H4)为________mol·L-1·min-1。
②上述条件下,该反应的平衡常数K为____________。
(5)丁烷-空气燃料电池以熔融的K2CO3为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的负极反应式为______________________________。
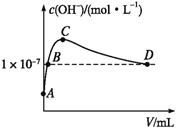
(6)K2CO3可由二氧化碳和氢氧化钾溶液反应制得。常温下,向1 L pH=10的KOH溶液中持续通入CO2,通入CO2的体积(V)与溶液中水电离出的OH-浓度的关系如图所示。C点溶液中各离子浓度大小关系为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用光洁铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察到火焰呈黄色。下列判断正确的是
A. 只含有Na+ B. 一定含有Na+,可能含K+
C. 既含有Na+,又含K+ D. 可能含有Na+,可能含有K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,Cu2+,Mn2+、Fe2+、Zn2+等四种金属离子(M2+)形成硫化物沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列有关判断不正确的是
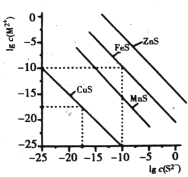
A. 该温度下,Ksp(MnS)大于1.0×10-15
B. 该温度下,溶解度:CuS>MnS>FeS>ZnS
C. 向含Mn2+、Zn2+的稀溶液中滴加Na2S溶液,Mn2+最有可能先沉淀
D. 向c(Fe2+)=0.1mol/L的溶液中加入CuS粉末,有FeS沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水体污染的治理是化学工作者研究的重要课题。
(1)水体常见污染物之一的氨氮主要指游离氨或铵盐,可以通入一定量的氯气,利用产生的HC1O除去。
已知:NH4++HClO=NH2Cl+H++H2O △H=akJ/mol
2NH2Cl+HClO=N2+H2O+3H++3Cl- △H=bkJ/mol
NH4++4HClO=NO3-+6H++4Cl-+H2O △H=ckJ/mol
则2NH4++3HClO=N2+3H2O+5H++3Cl- △H=______kJ/mol
(2)电解法也可除去水中的氨氮,实验室用石墨电极电解一定浓度的(NH4)2SO4与NaCl的酸性混合溶液来模拟。
①电解时,阳极的电极反应式为______________。电解过程中溶液初始Cl-浓度和pH对氨氮去除速率与能耗(处理一定量氨氮消耗的电能)的影响关系如图1和图2所示:
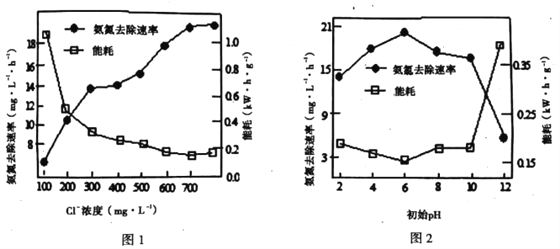
②图l中当Cl-浓度较低时、图2中当初始pH达到12时,氨氮去除速率低而能耗高的原因可能是_______________________。
③图2中,pH为____时处理效果最佳;当pH过低时,处理效果不佳的原因可能是_______。
(3)废水中的重金属离子通常用沉淀法除去。已知Ksp(NiS) =1.1×l0-21.Ksp(CuS)=1.3×10-36,国家规定的排放标准:镍低于1.1×10-5mol/L,铜低于7.8×l0-5mol/L。则需要控制溶液中S2-的浓度不低于______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某人设计淀粉利用方案如下图所示:
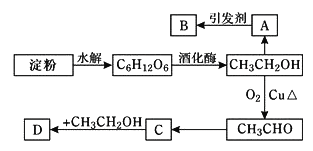
已知:A是乙烯能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:
(1)A的电子式为_____________;
(2)写出下列转化的化学方程式:
①C→D:___________________,②CH3CH2OH→CH3CHO:____________________。
II.某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
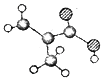
(3)该物质的分子式为______,该物质中所含官能团的名称为_______。
(4)写出该物质生成高分子的化学方程式:________________________。
(5)下列物质中,与该物质互为同分异构体的是________
①CH3CH=CHCOOH ②CH3CH(CH3)COOH ③CH3CH2CH=CHCOOH ④CH2=CHCOOCH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com