
【题目】已知:① ②
②![]()
现用丙二酸等物质合成含有小环的有机物K,合成路线如下:
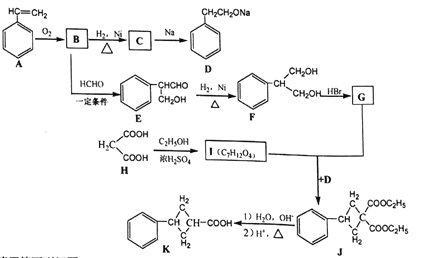
请回答下列问题:
(1)A的名称是_______,E中含氧官能团的名称是_____。
(2)B→C 的反应类型是_______ ,F→G的反应类型是____。
(3)G和I的结构简式分别为_______、________。
(4)写出F和H在一定条件下合成高分子化合物的化学反应方程式:_______。
(5)同时满足下列条件的E的同分异构体数目为________种。
① 能发生银镜反应;② 能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应。
(6)请写出以H2C=CHCH2Br为原料制备![]() ,参考本题题干写出制备的合成线路流程图(无机试剂任选)。________
,参考本题题干写出制备的合成线路流程图(无机试剂任选)。________
【答案】 苯乙烯 醛基和羟基 加成反应(或还原反应) 取代反应 ![]()
![]()
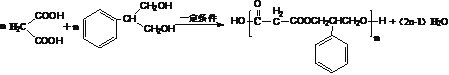 9
9 ![]()
【解析】由C和Na反应生成D(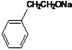 )则C结构简式为
)则C结构简式为![]() ,B与氢气反应得到C,B的结构简式为
,B与氢气反应得到C,B的结构简式为 ,B与HCHO反应是已知反应,F与HBr反应是醇—OH被Br原子取代生成G是
,B与HCHO反应是已知反应,F与HBr反应是醇—OH被Br原子取代生成G是![]() ,H与C2H5OH在浓H2SO4条件下反应为酯化反应,则I为
,H与C2H5OH在浓H2SO4条件下反应为酯化反应,则I为![]() ,E的同分异构体是甲酸酚酯,同分异构体如下:
,E的同分异构体是甲酸酚酯,同分异构体如下: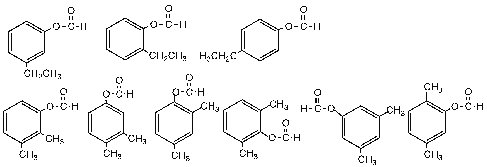 共有9种。
共有9种。
(1)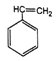 的名称是苯乙烯,
的名称是苯乙烯,![]() 中含氧官能团的名称是醛基和羟基;
中含氧官能团的名称是醛基和羟基;
(2)B与氢气发生加成(或还原)反应得到C,F与HBr反应是醇—OH被Br原子取代反应生成![]() ;
;
(3)由分析可知G和I的结构简式分别为![]() 、
、![]() 。
。
(4) 和
和![]() 在一定条件下发生缩聚反应生成高分子化合物的化学反应方程式为
在一定条件下发生缩聚反应生成高分子化合物的化学反应方程式为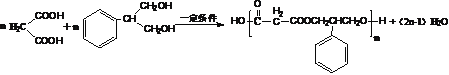 ;
;
(5)① 能发生银镜反应说明分子结构中含有醛基;② 能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应说明含有酯基,且是羧基苯酯,则分子结构中应该含有HCOO—,另外苯环上可能有一个—CH2CH3或二个甲基;满足条件的![]() 的同分异构分别为
的同分异构分别为 ,共有9种
,共有9种
(6)以H2C=CHCH2Br为原料制备![]() 合成线路流程图(无机试剂任选)为
合成线路流程图(无机试剂任选)为![]() 。
。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列有关叙述正确的是
A. 标准状况下,22.4LHF中含有的分子数为NA
B. 常温常压下,硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA
C. 标准状况下,8.96L平均相对分子质量为3.5的H2与D2含有的中子数为0.3NA
D. 0.1L18mol/L浓硫酸与足量金属铜在加热条件下充分反应,生成0.9NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1mol·L-1的氨水中逐渐加入等浓度的盐酸,溶液中pOH [pOH=-lgc(OH-)]与pH的变化关系如下图所示.下列说法不正确是
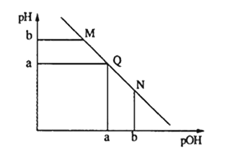
A. M点和N点溶液中H2O的电离程度相同
B. Q点溶液中,c(NH4+)+c(NH3·H2O)=c(Cl-)
C. M点溶液的导电性小于Q点溶液的导电性
D. N点溶液加水稀释,![]() 变小
变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如下图所示。

请回答下列问题:
(1)A的结构简式为 ,反应②的化学方程式为 。
(2)反应⑦中物质X的分子式为 ,反应⑧的类型为 。
(3)反应⑤的化学方程式为 。反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是 。
(4)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为 。
(5)请补充完整证明反应①是否发生的实验方案:取反应①的溶液2 mL于试管中 。(实验中可供选择的试剂:10%的NaOH溶液、5%的CuSO4溶液、碘水)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)(已知:2SO2+O2![]() 2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )
2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )
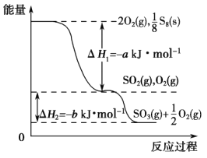
A.S8的燃烧热 ΔH=-a kJ·mol-1
B.1 mol SO2和过量 O2反应可释放出 b kJ 的热量
C.已知1个S8分子中有8个S-S,S=O的键能为d kJ·mol-1,O=O的键能为e kJ·mol-1,则S8分子中S-S的键能为(2d-a-e) kJ·mol-1
D.若使用V2O5作催化剂,当SO2(g)转化生成1mol SO3(g)时,释放的热量小于b kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是A、B、C、D、E五种有机物的有关信息:

根据表中信息回答下列问题:
(1)A到E中,属于烃的是_______(填字母);写出A与溴水反应的化学方程式_____________。
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式_______。当n=________时,这类有机物开始出现同分异构体。
(3)B具有的性质是_____________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤任何条件下不与氢气反应⑥可使酸性高锰酸钾溶液和溴水均褪色
(4)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:_________________。
(5)C与E反应能生成相对分子质量为100的酯,该反应类型为_____________;其化学方程式为:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式是Fe+2Fe3+=3Fe2+ , 该原电池的组成正确的是( )
Zn | A | B | C | D |
正极 | Fe | C(石墨) | Ag | Zn |
负极 | Cu | Fe | Fe | Fe |
电解质溶液 | FeCl3 | Fe2 (SO4)3 | H2SO4 | FeCl3 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂,工业上可通过吸收大气污染物(含有SO2、NO等制取),同时还可得到NH4NO3产品,工艺流程图如下(Ce为铈元素):

请回答下列问题:
(1)装置I中可生成NaHSO3。常温下NaHSO3溶液呈酸性的原因是____________。
(2)装置II中酸性条件下,NO被Ce4+氧化为NO3- 时,氧化产物与还原产物的物质的量之比为______。
(3)装置III中阴极上的电极反应式为__________。若装置IV中NO2- 的浓度为11.5g·L-1要使1dm3该
溶液中的NO2- 完全转化为NH4NO3,至少向装置IV中通入标准状况下的O2__________L。
(4)Na2S2O4在空气中容易被氧化,其反应方程式可能为:
①2Na2S2O4+O2+2H2O=4NaHSO3;
②Na2S2O4+O2+H2O=NaHSO3+ NaHSO4。
请设计实验证明氧化时一定有反应②发生______________。
(5)SO2—空气质子交换膜燃料电池原理示意图如下图:

质子的流动方向为__________(“从A到B”或“从B到A”),负极的电极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于生物体内水和无机盐的叙述,错误的是
A. 是细胞中能源物质之一
B. 哺乳动物血液中钙离子含量过少会引起抽搐
C. 细胞内的自由水是生化反应的重要介质
D. 铁是合成血红蛋白的原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com