
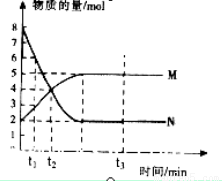
һ���¶��£����ݻ�ΪVL���ܱ������н��з�Ӧ��aN(g) bM(g)��N��M�����ʵ�����ʱ��ı仯������ͼ��ʾ��
bM(g)��N��M�����ʵ�����ʱ��ı仯������ͼ��ʾ��
��1���˷�Ӧ�Ļ�ѧ����ʽ�� =________��
=________��
��2��t1��t2ʱ�̣���M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ_________��
��3��������������˵��������Ӧ�ﵽƽ��״̬����________��
A ��Ӧ��M��N�����ʵ���֮��Ϊ1:1
B ������������������ʱ��ı仯���仯
C �������������ʵ�������ʱ��ı仯���仯
D ��λʱ����ÿ����a mol N��ͬʱ����b mol M
E����������ѹǿ����ʱ��ı仯���仯
F��N�����������ڻ�������б��ֲ���
(6�֣�ÿ��2��)��1��2����2��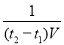 mol��L-1��min-1����3��CEF(��2����1�֣��д�������)
mol��L-1��min-1����3��CEF(��2����1�֣��д�������)
��������
���������1����ͼ���֪���ӿ�ʼ��ƽ�⣬��n(N)=8mol-2mol=6mol����n(M)=5mol-2mol=3mol���ʴ˷�Ӧ�Ļ�ѧ����ʽ��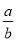 =
=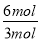 =2��
=2��
��2��t1��t2ʱ�̣���M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊv(M)= 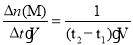 mol��L-1��min-1��
mol��L-1��min-1��
��3��A����Ӧ��M��N�����ʵ���֮��Ϊ1:1���Ƿ�Ӧ���̵�һ��״̬������ȷ���Ƿ�ﵽƽ�⣻B�����۷�Ӧ������Σ�������������������仯����B�����жϣ�C������Ӧ����������У��������������ʵ�����С���������ʵ�������ʱ��ı仯���仯����ﵽƽ�⣻D����λʱ����ÿ����a mol N��Ϊ�����ʣ�ͬʱ����b mol M��Ϊ�����ʣ����������ʣ������жϣ�E���������������ʵ�����С����������ѹǿ��С������������ѹǿ����ʱ��ı仯���仯����˵���Ѿ��ﵽƽ�⣻F������Ӧ����������У�N�������������٣������ڻ�������б��ֲ��䣬��˵���Ѿ��ﵽƽ�⡣
���㣺���ʵ����仯ͼ���뷴Ӧ�������Ĺ�ϵ����Ӧ���ʵļ��㡢���淴Ӧ�ﵽƽ��ı�־�жϡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
A��B��C��D���Ǻ�̼���⡢���ĵ������Ż����Aˮ���B��C��B�������Եõ�C��D��D����Ҳ�õ�C����M(X)��ʾX��Ħ������������ʽ����ȷ���ǣ� ��
A��M(A)=M(B)+M(C) B��2M(D)= M(B)+M(C)
C��M(B)< M(D)��M(C�� D��M(D)��M(B)<M(C) ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����и߶���ѧ���������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʽΪC5H12������������ں�3�����������Ķ��ȴ����ͬ���칹�����ĿΪ
A.8�� B.9�� C.10�� D.11��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���������ʵ���Ũ�Ⱦ���ȵ�������Һ��
������ڴ���۰�ˮ����CH3COONa��Һ������˵����ȷ����
A��������ڷֱ�ϡ����ͬ��������Һ��pH����>��
B��������ۻ�Ϻ���Һ�����ԣ����ڳ�����Ka(CH3COOH)=Kb(NH3?H2O)
C����������ѵ����ˮ���ӵ���Ŀ���
D������ܻ��������Һ�����ԣ���c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����и�һ��ѧ���������Ի�ѧ��A�����Ծ��������棩 ���ͣ������
ij��ѧ��ȤС��Ϊ��̽�����缫��ԭ����е����ã���Ʋ�������һϵ��ʵ�飬ʵ������¼���£�

������ϱ��е�ʵ���¼�ش��������⣺
��1��ʵ��1��2�е�Al�����ĵ缫�Ƿ���ͬ��____________________��
��2����ʵ��3�У�Al��__________�����缫��ӦʽΪ___________������ܷ�ӦʽΪ__________��
��3��ʵ��4�е�Al���������Ǹ�����____________________��ԭ����____________________��
��4������ʵ��5�е�����ָ��ƫ��Al��ԭ��__________________��
��5������ʵ�������ܽ���ԭ����н��������������Ǹ����ܵ���Щ���ص�Ӱ�죿____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����и�һ��ѧ���������Ի�ѧ��A�����Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A����NH4HCO3��Һ�мӹ���Ca(OH)2��Һ��HCO3-+OH-+Ca2+=CaCO3��+H2O
B���ö��Ե缫MgCl2���ˮ��Һ��2Cl-+2H2O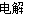 Cl2��+H2��+2OH-
Cl2��+H2��+2OH-
C����ƫ��������Һ�м�����������������Һ��2AlO2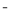 +H
+H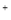 +H2O=Al(OH)3��
+H2O=Al(OH)3��
D��Ũ������������̻�Ϲ��ȣ�MnO2+4H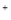 +4Cl
+4Cl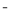 =Mn
=Mn +2H2O+2Cl2��
+2H2O+2Cl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����и�һ��ѧ���������Ի�ѧ��A�����Ծ��������棩 ���ͣ�ѡ����
��ҵ�������е�һ����Ҫ��Ӧ��SO2(��400-500 C�µĴ�������2SO2+O2
C�µĴ�������2SO2+O2 2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���������
2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���������
A�������������£�SO2����100%��ת��ΪSO3
B��ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч��
C���ﵽƽ��ʱ��SO2��SO3��Ũ�ȱ��ֲ���
D��Ϊ�����SO2��ת���ʣ������ʵ����O2��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и����꼶�����ο������ۻ�ѧ�Ծ��������棩 ���ͣ������
��14�֣��о�CO2�����öԴٽ���̼���Ĺ���������Ҫ���塣
��1����CO2�뽹̿��������CO��CO�����������ȡ�
��֪����Fe2O3(s) + 3C(ʯī) = 2Fe(s) + 3CO(g) ��H 1 = +489��0 kJ��mol��1
��C(ʯī) +CO2(g) = 2CO(g) ��H 2 = +172��5 kJ��mol��1
��CO��ԭFe2O3(s)���Ȼ�ѧ����ʽΪ ��
��2��������̼�ϳɼ״���̼���ŵ��·���CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��
CO2(g) +3H2(g) CH3OH(g) +H2O(g) ��H
CH3OH(g) +H2O(g) ��H
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪK= ��
��ȡһ�����CO2��H2�Ļ�����壨���ʵ���֮��Ϊ1��3������������ܱ������У�����������Ӧ��Ӧ�����в�ü״������������(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ��ͼ1��ʾ����÷�Ӧ�Ħ�H 0 ���>������<����������
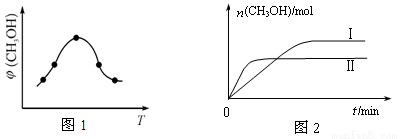
�������ֲ�ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ2��ʾ������I�����Ӧ��ƽ�ⳣ����С��ϵΪK�� K��(�>������<������)��
��3����CO2Ϊԭ�ϻ����Ժϳɶ������ʡ�
�ٹ�ҵ������[CO(NH2)2]��CO2��NH3��һ�������ºϳɣ��䷴Ӧ����ʽΪ ��
����̼��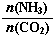 ��3����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ�� ��
��3����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ�� ��
����������Һ������ʽ��е�⣬CO2�ڵ缫�Ͽ�ת��Ϊ���飬�õ缫��Ӧ�ķ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��������ѧ�����п��Ը߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
��7�����ʣ��ټ���ڱ��۾���ϩ����ϩ��������ױ� ����ϩ��
��Ϊ������ѧ��Ӧ������ʹ���Ը��������Һ��ɫ����ʹ��ˮ��ɫ����
A���ۢܢ� B���ܢݢ� C���ܢ� D���ܢޢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com