
重铬酸钾(K2Cr2O7)是常用的氧化剂,工业上以铬铁矿(含有Cr2O3、FeO、Al2O3、SiO2等)为原料制备重铬酸钾的流程如下。
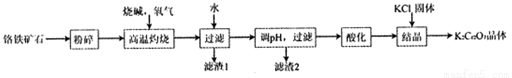
已知:NaFeO2遇水强烈水解。
请回答下列问题:
(1)将矿石粉碎的目的是_________。
(2)高温灼烧后产物中含有NaFeO2、Na2CrO4等成份,写出生成Na2CrO4的化学方程式____________。
(3)“滤渣1”中有红褐色物质,写出生成该物质的离子方程式______________。
(4)“滤渣2”中主要成分是A1(OH)3和 ___________。
(5)“酸化”反应的离子方程式为2CrO42-(aq)+2H+(aq) Cr2O72-(aq)+H2O。在25℃时,取Na2CrO4溶液进行酸化实验,测得部分实验数据如下:
Cr2O72-(aq)+H2O。在25℃时,取Na2CrO4溶液进行酸化实验,测得部分实验数据如下:
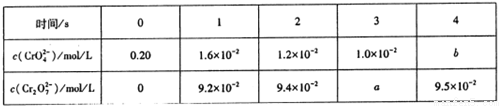
表格中b=__________;若反应达到平衡时,溶液的pH=1,则该反应的平衡常数K=__________;
(6)简要说明Na2CrO7溶液中加入KCl固体,“结品”析出K2Cr2O7晶体的原因_________________。
科目:高中化学 来源:2016-2017学年浙江省杭州市五校高一上学期联考化学试卷(解析版) 题型:选择题
下列物质在水中的电离方程式书写正确的是
A.NaHSO4 =Na++HSO4- B.NaHCO3 =Na++H++CO32-
C.KClO3 =K++Cl-+3O2- D.Al2(SO4)3 =2Al3++3SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市宝坻区高二11月联考化学试卷(解析版) 题型:选择题
在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g)?C(g)+D(g),5min后达到平衡,各物质的平衡浓度的关系为:ca(A)•c(B)=c(C)•c(D).若在温度不变的情况下将容器的体积扩大为原来的5倍,A的转化率不发生变化,则B的转化率为( )
A.60% B.40% C.4% D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二12月月考化学试卷(解析版) 题型:填空题
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g) K1 △H1<0(I)
2NO(g)+Cl2(g)?2ClNO(g) K2 △H2<0(II)
(1)4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g) K3 △H3
K3 = (用K1、K2表示)(K1、K2、K3均为平衡常数)
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入 0.2mol的NO和0.1mol的 Cl2,10min时反应(II)达到平衡。测得10min内 V(ClNO)= 7.5×10—3mol/(L•min),则平衡后 n(Cl2)= mol,NO的转化率a1= 。 其他条件不变,反应(II)在恒压条件下进行,平衡时NO的转化率a2 a1(填“>”、“<”或“=”), 平衡常数K2 (填“增大”、“减小”或“不变”)。若要使K2减小,可采取的措施是__________________。
(3)实验室可用NaOH溶液吸收NO2,反应为 2NO2 + 2 NaOH = NaNO3 + NaNO2 + H2O。含0.2mol NaOH的水溶液与 0.2mol NO2恰好完全反应得 1L溶液A,溶液B 为 0.1mol/L的CH3COONa溶液,则两溶液中 c(NO3—)、c(NO2—)、和c(CH3COO—)由大到小的顺序为______________________(已知 HNO2的电离常数为 Ka= 7.1×10—4mol/L,CH3COOH的电离常数为 Ka= 1.7×10—5 mol/L )可使溶液A和溶液B的PH相等的方法是
Ka= 1.7×10—5 mol/L )可使溶液A和溶液B的PH相等的方法是
A、向溶液A中加适量水 B、向溶液A中加适量Na OH
OH
C、向溶液B中加适量水 D、向溶液B中加适量NaOH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二12月月考化学试卷(解析版) 题型:选择题
用NA表示阿伏伽德罗常数,下列叙述 正确的是 ( )
正确的是 ( )
A、2L 0.5mol/L的硫酸钾溶液中阴离子所带电荷数 为2NA
为2NA
B、2L 0.5mol/L的Na2CO3溶液中,CO32—的数目为 NA
C、1L 0.5mol/L的CH3COOH溶液中含有的H+数目为 NA
D、2L 0.1mol/L的NH4Cl溶液中 NH4+和NH3• H2O的数目之和为 0.2NA
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三新考试大纲适应性考试化学卷(解析版) 题型:选择题
如图为元素周期表短周期的一部分,Z原子的电子层数为n,最外层电子数为2n+1。下列叙述错误的是
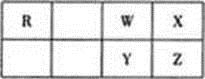
A. X和Z氢化物的热稳定性和还原性均依次减弱
B. R、W和氢三种元素形成的阴离子有2种以上
C. RY2分子中每个原子的最外层均为8电子结构
D. R、Y、Z的最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第三次阶段测化学试卷(解析版) 题型:填空题
分B、C、D、E、F 是原子序数依次增大的短周期主族元素,B 是短周期中金属性最强的 元素,C 是同周期中离子半径最小的元素,D 元素的最高价氧化物对应水化物与 B 元素的最高 价氧化物对应水化物反应的产物 M 是制备木材防火剂的原料,E 的最外层电子数与内层电子数 之比为 3﹕5。请回答:
(1)D 的原子结构示意图为___________________。
(2)写出工业制 F 单质的化学方程式:___________________。
(3)用电子式表示元素 B 与元素 F 形成的化合物:___________________。
(4)B单质与氧气反 应的产物与 C 的单质同时放入水中,产生两种无色气体,有关的化学方程式为____________________、___________________。
(5)写出 M 与盐酸反应的离子方程式:___________________。
(6)工业上将干燥的 F 单质通入熔融的 E 单质中可制得化合物 E2F2,该物质可与水反应生成 一种能使品红溶液褪色的气体,0.2mol 该物质参加反应时转移 0.3mol 电子,其中只有一种元素化合价发生改变,该反应的化学方程式为___________________。
查看答案和解析>>
科目:高中化学 来源:2017届广西省钦州市钦州港区高三12月月考化学试卷(解析版) 题型:选择题
下列实验操作正确的是
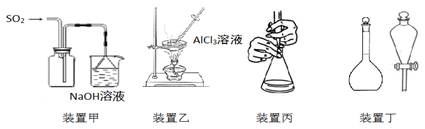
A. 用装置甲收集SO2
B. 用装置乙制备AlCl3晶体
C. 用装置丙进行中和滴定时,滴定前锥形瓶先用待装液润洗
D. 装置丁中使用分液漏斗和容量瓶时,先要检查仪器是否漏液
查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高二上期末化学卷(解析版) 题型:选择题
下列有关问题,与盐的水解有关的是( )
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
⑥HF水溶液不能用玻璃试剂瓶盛装
A.①②③ B.②③④ C.①②③④⑤ D.①②③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com