
| A. |  | B. |  | C. | 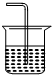 | D. | 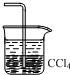 |
分析 为使生成的氨气被硫酸吸收时不发生倒吸,则使气体与水不能直接接触或装置中具有球形结构、倒扣的漏斗等,以此来解答.
解答 解:A.倒扣在液面的漏斗可以防止倒吸,利用倒吸液体自身重量回落,图中装置不发生倒吸,故A不选;
B.干燥管具有球形结构,上部面积较大,倒吸的液体可以靠自身质量能回落避免倒吸,故B不选;
C.导气管直接插入液体,气体极易溶解于水,会沿导气管倒吸到发生装置,故C选;
D.氨气不溶于四氯化碳,四氯化碳的密度比水大在下方,先通过四氯化碳后再通过硫酸可以吸收氨气,氨气不和硫酸溶液接触避免了倒吸,故D不选;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、防止倒吸的原理为解答的关键,侧重分析与实验能力的考查,注意仪器及装置的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
 和
和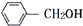 互为同系物,均可以与金属钠反应.
互为同系物,均可以与金属钠反应.| A. | .③④⑤⑥ | B. | ①②③④ | C. | ①②⑤⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.6 mol/(L•min) | B. | v(B)=1.2 mol/(L•min) | ||
| C. | v(C)=1.2 mol/(L•min) | D. | v(B)=0.03 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸钠与碳酸氢钠的混合溶液逐滴滴入盐酸溶液,立即产生大量气泡 | |
| B. | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明该溶液中有SO42- | |
| C. | 常温下,向0.1mol/L NaF和pH=12 NaOH的混合溶液中,滴加MgCl2溶液,先生成 MgF2沉淀(已知K[Mg(OH)]2=7.4×10-11 K( MgF2)=5.6×10-12) | |
| D. | 向 Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,则溶液变黄,说明氧化性H2O2>Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4 | B. | Na2SO4 | C. | CuCl2 | D. | NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| a | b | c | |
| I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
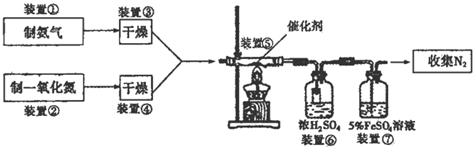

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com