
将250 mL含BaCl2和KCl的混合溶液分成10等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则原混合溶液中钾离子物质的量浓度为
A.4(b-2a)mol/L B.20(2a-b)mol/L
C.20(b-2a)mol/L D.40(b-2a)mol/L
科目:高中化学 来源:2016-2017学年河北省高一12月月考化学卷(解析版) 题型:选择题
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.分别加热这两种固体物质,并将生成的气体通入澄清的石灰水中
B.分别在这两种物质的溶液中,加入CaCl2溶液
C.分别在这两种固体中,加入同浓度的稀盐酸
D.分别在这两种物质的溶液中,加入少量澄清的石灰水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市部分区高二上学期期末化学试卷(解析版) 题型:实验题
某化学小组利用硫代硫酸钠进行了相关的实验。
Ⅰ.已知:Na2S2O3 + H2 SO4 Na2SO4 + SO2↑+S↓+H2O,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(1)该实验①、②可探究温度对反应速率的影响,因此V1=V2 =________,V3=_______;
(2)若V4=10.0,V5=6.0,则实验①、③可探究__________对反应速率的影响。
Ⅱ.利用反应:I2+2Na2S2O3 Na2S4O6+2NaI可定量测定硫代硫酸钠(Mr=158)的纯度,现在称取wg硫代硫酸钠固体样品,配成250 mL的溶液,取25.00 mL置于锥形瓶中,加入指示剂,用a mol/L的碘水滴定,消耗碘水b mL,则:
(3)滴定应选择的指示剂是_________,滴定终点的现象为____________________
________________________。
(4)对于该滴定实验的有关操作或误差分析正确的是____________。
a.滴定前,要用对应装入的溶液润洗锥形瓶和滴定管
b.滴定过程中,标准液滴到锥形瓶外, 会使所测得的结果偏大
会使所测得的结果偏大
c.滴定开始时滴定管尖嘴有气泡,滴定结束后气泡消失,测得纯度将偏小
d.滴定前仰视读数而滴定结束时平视读数,则所测得的纯度将会偏小
(5)样品中硫代硫酸钠纯度的表达式为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市部分区高二上学期期末化学试卷(解析版) 题型:选择题
常温时0.1 mol/L CH3COONa溶液中各离子浓度排序正确的是
A.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高一上学期期末化学试卷(解析版) 题型:填空题
硅酸钠被国家列为“我国优先发展的精细化学品”和“今后我国无机化工 产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
产品发展重点”之一。下图是用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的工艺流程示意简图:
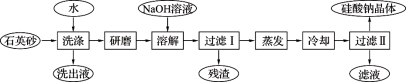
(1)要将洗出液中的溶质析出,采用的方法是 (填“蒸发”、“降温”)结晶;操作时用到的硅酸盐仪器有酒精灯(再填2个仪器) 。
(2)残渣的主要成分为: 。
(3)上述流程中加入NaOH溶液,反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高一上学期期末化学试卷(解析版) 题型:选择题
下列操作,发生“先产生沉淀,然后沉淀又溶解”现象的是
①金属钠投入到FeCl3溶液中
②向NaAlO2溶液中逐滴加入过量的稀盐酸
③澄清石灰水溶液中缓慢通入二氧化碳至过量
④向硅酸钠溶液中逐滴加入过量的盐酸
A.①② B.①③ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高一上学期期末化学试卷(解析版) 题型:选择题
工业上曾经通过反应“3Fe+4NaOH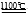 Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是
Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是
A.不能用磁铁将Fe与Fe3O4分离
B.将生成的气体在空气中冷却可获得钠
C.该反应条件下铁的氧化性比钠强
D.该反应中每生成2 mol H2,转移的电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高二上学期期末化学试卷(解析版) 题型:选择题
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+O2(g)  2SO3(g)并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3(g)并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
A.等于p% B.大于p% C.小于p% D.无法判断
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高一上学期期末化学试卷(解析版) 题型:选择题
下列实验操作或事故处理正确的是
A. 金属钠着火,立即用水扑灭
B. 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中
C. 实验结束后,用嘴吹灭酒精灯
D. 皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com