
【题目】下列说法中正确的是( )
A. 氮气和氢气在点燃或光照条件下可合成氨
B. 氨水显碱性,能使石蕊溶液变红色
C. 氨气遇到浓盐酸会发生反应而产生白烟
D. 由氨制取硝酸过程中,氮元素被还原
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在400℃、101 kPa时,NO2(g) +CO(g) ![]() NO(g) + CO2(g) 反应过程的能量变化如下图所示。
NO(g) + CO2(g) 反应过程的能量变化如下图所示。
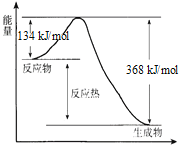
反应过程
(1)该反应是_____________(填“吸热”或“放热”)反应。
(2)该反应的热化学方程式为_____________。
(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是_____________。
a.浓度 b.压强 c.温度 d.催化剂
(4)反应体系中加入催化剂对反应热是否有影响?____(填“是”或“否”),原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.简单离子的半径先减小后增大,卤素离子半径最大
b.元素金属性减弱,非金属性增强
c.最高价氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点逐渐降低
(2)原子最外层电子数是次外层电子数一半的元素名称为____,还原性最弱的简单阴离子是____。
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 共价化合物 | |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是________________________________,根据熔点推测Al2O3是___________化合物。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗)![]() SiCl4
SiCl4![]() SiCl4(纯)
SiCl4(纯)![]() Si(纯)
Si(纯)
写出SiCl4的电子式:_____________,在上述由SiCl4(g)制纯硅的反应中,测得每生成0.56 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:_____________________________________________。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,但可用P2O5干燥的是_________。
a.HI b.NH3 c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各说法中,正确的是
A. 对于2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反应中充入1mol SO2和足量的氧气反应时,放出的热量一定是Q/2 kJ
2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反应中充入1mol SO2和足量的氧气反应时,放出的热量一定是Q/2 kJ
B. 热化学方程式中的化学计量数不能用分数表示
C. Zn(s)+H2SO4(aq) ===ZnSO4(aq)+H2(g) ΔH<0,该反应的化学能可以转化为电能
D. ΔH的大小与热化学方程式的化学计量数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg、Al、Fe三种金属的混合物与足量的稀硫酸反应,生成2.80 L H2(标准状况),则三种金属的物质的量之和不可能是( )
A. 0.120 mol B. 0.110 mol C. 0.080 mol D. 0.100 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将晶体X加热分解,可得A、B、D、E、F和H2O六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1) A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式: ________________________。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是____________________。
(3)E能使湿润的红色石蕊试纸变蓝,E的结构式为__________________,工业制取E气体的化学方程式为___________________________。
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为____________________、____________________、__________________。
(5)取一定量的X晶体分解,若生成0.1mol F,则必同时生成____________(填化学式)________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组用右图装置进行实验,试回答:
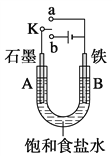
(1)若开始时开关K与a连接,则A电极反应式为___________________。
(2)若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做________________,则A电极反应式为_____________________;B电极反应式为_________________________。
(3)开关K与b连接,将饱和食盐水换成CuSO4溶液,则A电极反应式为___________,该反应的离子方程式为______________________________ ,电解一段时间后(溶液仍然为蓝色),溶液的pH值将_________(填“变大”、“变小”、“不变”),若将电解质溶液恢复至原状,应补充_____________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com