
下面提到的情况中,与盐的水解有关的是
①明矾和FeCl3可作净水剂②为保存FeCl3溶液,要在溶液中加少量盐酸③实验室配制AlCl3溶液时,应先把它溶解在盐酸中,而后加水稀释④NH4Cl溶液可作焊接中的除锈剂⑤实验室盛放Na2SiO3溶液的试剂瓶应用橡皮塞,而不能用玻璃塞⑥用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂⑦在NH4Cl或AlCl3溶液中加入金属镁会生成氢气⑧草木灰与铵态氮肥不能混合施用⑨加热蒸干AlCl3溶液得到Al(OH)3固体
A.①④⑦ B.②⑤⑧ C.③⑥⑨ D.全部
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源:2016-2017学年甘肃省高二上阶段考二文化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.控制塑料购物袋的使用主要是为了节约成本
B.使用可降解塑料袋有利于减少“白色污染”
C.聚氯乙烯塑料袋可用来长时间存放食品
D.塑料购物袋具有热固性,不能回收利用
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上期中化学卷(解析版) 题型:填空题
铁和铝是两种重要的金属,它们的单质及其化合物有着各自的性质。
(1)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为________________;铁在高温条件下与水蒸气反应的化学方程式为______________。
(2)某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的一种或几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。(已知:Al(O H)3 + NaOH = NaAlO2 + 2H2O)回答下列问题:
H)3 + NaOH = NaAlO2 + 2H2O)回答下列问题:

①溶液中一定含有的溶质是____________ (填化学式)。
②溶液中可能含 有的溶质是_________ (填名称),判断该物质是否存在的实验现象是____________。
有的溶质是_________ (填名称),判断该物质是否存在的实验现象是____________。
③分别写出AB段、BC段发生反应的离子方程式:
AB段为________________________________;
BC段为________________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上期中化学卷(解析版) 题型:选择题
1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为
A.64 g B.64 C.64 g/mol D.32 g/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上期中化学卷(解析版) 题型:填空题
已知25 ℃时部分弱电解质 的电离平衡常数数据如表所示,回答下列问题:
的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 |
|
电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1 mol·L-1的下列四种溶液,pH由小到大排列的顺序是 (用编号填写)。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1 mol·L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 (填字母)。
A.c(H+)
B.
C.c(H+)·c(OH-)
D.
E.
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式 。
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH3COO-)-c(Na+)= (填准确数值)。
(5)25℃时,将a mol·L-1的醋酸与b mol·L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离常数为_________。

(6)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离平衡常数___________(填“>”、”=”或“<”)CH3COOH的电离平衡常数。
(7)标准状况下,将1.12 L CO2通入100 mL 1 mol·L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
①c(OH-)=2c(H2CO3)+_____________________。
②c(H+)+c(Na+)=________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是
A.在一定温度下,AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数
B.AgCl的Ksp=1.8×10-10mol2·L-2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10mol2·L-2
C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ks p值时,此溶液为AgCl的饱和溶液
p值时,此溶液为AgCl的饱和溶液
D.向饱和AgCl水溶液中加入盐酸,Ksp值变大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上期中化学卷(解析版) 题型:选择题
为了配制NH 的浓度与Cl-的浓度比为1∶1的溶液,可在NH4Cl溶液中加入
的浓度与Cl-的浓度比为1∶1的溶液,可在NH4Cl溶液中加入
①适量的盐酸 ②适量的NaCl ③适量的氨水④适量的NaOH
A.①② B.③ C.③④ D.④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省武汉外国语学校高一上期中化学卷(解析版) 题型:实验题
实验室里从海藻中提取碘的流程图如图1所示:
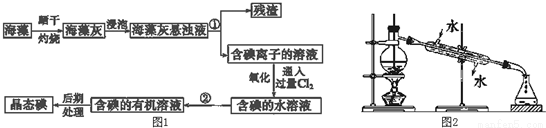
(1)指出制取碘的过程中有关的实验操作名称:①___________,②___________.操作②中要用 到分液漏斗,在使用分液漏斗前要检查是否漏水,检查方法是_______________
到分液漏斗,在使用分液漏斗前要检查是否漏水,检查方法是_______________
(2)灼烧海藻时,除需要三脚架外,还需要用到的仪器是___________(从下列仪器中选择所需的仪器,将标号字母填写在空白处).
A烧杯 B坩埚 C表面皿 D泥三角 E酒精灯 F干燥器
(3)提取碘的过程中,可供选择的有机溶剂是___________(填字母序号).
A.酒精 B.四氯化碳 C.苯 理由是____________________
(4)进行上述蒸馏操作时,最后晶体碘在___________里聚集.
(5)含碘的有机物溶液中提取碘和回收有机溶剂,还需要经过蒸馏,观察如图2实验装置,指出其错误之处,并指出正确操作___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中必修化学卷(解析版) 题型:填空题
⑴合理膳食、均衡营养是保证人体健康和生活质量的重要途径。
① 人体必需的元素摄入不足会影响人体的正常生理活动。下列做法不能达到目的的是 。
a.补碘——食用加碘盐
b.补铁——使用铁强化酱油
c.补钙——服用葡萄糖
② 人体内有8种氨基酸必需通过食物摄入,某品牌饼干含有的下列物质中能转化为氨基酸的是 。
a.纤维素 b.蛋白质 c.油脂
③ 人类历史上最重要的抗生素是 。
a. 青霉素 b.维生素 c.胡萝卜素
⑵ 构建人与自然的和谐、营造安全的生态环境已成为全人类的共识。
① 如图Ⅰ,向两只250mL的锥形瓶中分别充入CO2和空气,用白炽灯泡照射一段时间后,其中a瓶中温度计读数稍低,则盛放CO2的锥形瓶为 (填“a”或“b”)。

图Ⅰ 图Ⅱ
② 为防止白色污染,废旧的塑料需投入到贴有图II标志的垃圾桶内,该标志表示的是 。
③ 废水中铊(Tl)具有高毒性,治理时常加入NaClO溶液,将Tl+转变为Tl3+,NaClO作
(填“氧化剂”或“还原剂”),同时加入适量氨水,将Tl3+转变为难溶物Tl(OH)3,写出生成Tl(OH)3的离子方程式 。
⑶ 材料是人类社会发展的物质基础,材料科学的发展离不开化学。
① 黏土是陶瓷的生产原料,其中江苏宜兴的高岭土是含有杂质较少的高品质黏土,其主要组成可表示为Al2Si2Ox(OH)4,则x= 。
② 2016年奥运会在巴西举行,场馆的建设需大量的建筑材料。其中生产水泥、玻璃共同的原料是 (填名称),场馆内的座椅通常用高密度聚乙烯(HDPE)为原料制得,聚乙烯属于 塑料(填“热固性”或“热塑性”)。
③ 沪通铁路建设正在积极推进,其中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一。铁在发生电化学腐蚀时的负极反应方程式为 。
④ 工业上常用SiCl4与O2在高温条件下通过置换反应制得SiO2,并于2000℃下拉成光纤细丝。该反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com