
下列有关氧化还原反应的叙述正确的是
A.肯定有一种元素被氧化,另一种元素被还原
B.在反应中应有沉淀、气体或水生成
C.置换反应一定属于氧化还原反应
D.化合反应和复分解反应有可能是氧化还原反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年吉林省德惠市高一上学期期中测试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.摩尔质量是1mol 物质的质量
B.胶体是一种带电荷的介稳体系
C.电解质不一定导电
D.氧化还原反应的本质是化合价升降
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:选择题
一定条件下的反应:PCl5(g)  PCl3(g)+Cl2(g)(△H>0)达到平衡后,下列情况使PCl5分解率降低的是
PCl3(g)+Cl2(g)(△H>0)达到平衡后,下列情况使PCl5分解率降低的是
A.温度、体积不变,充入氩气 B.体积不变,对体系加热
C.温度、体积不变,充入氯气 D.温度不变,增大容器体积
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上学期期中理综化学试卷(解析版) 题型:填空题
I.甲、乙两池电极材料都是铁棒与碳棒(如图)。请回答下列问题:
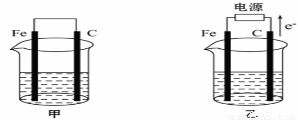
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的________棒;乙池中的________棒。
②在乙池中阴极的电极反应式是________________________________。
(2)若两池中均盛放饱和NaCl溶液。
①写出甲池中负极的电极反应式__________________________________。
②写出乙池中的总反应的离子方程式______________________________。
II.我国在青藏高原发现了名为“可燃冰”的环保型新能源。
(1)CH4可与Cl2反应,反应历程如下
①Cl2→2Cl ΔH = 243 kJ·mol-1
②Cl+CH4→CH3+HCl ΔH = 4 kJ·mol-1
③CH3+Cl2→CH3Cl+Cl ΔH = -106 kJ·mol-1
则CH4与Cl2反应生成CH3Cl(g)的热化学方程式为 __。
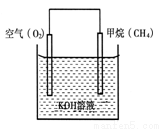
(2)CH4可用于设计燃料电池,甲烷燃料电池的工作原理如图所示:则通入CH4的一极为原电池的 (填“正极”或“负极”),负极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期期中测试化学试卷(解析版) 题型:选择题
欲配制100mL1.0mol/LCuSO4溶液,正确的方法是
A.将16.0g CuSO4溶于100mL水中
B.将25.0g CuSO4·5H2O溶于少量水中,再用水稀释至100mL
C.将20mL5.0mol/L CuSO4溶液用水稀释至100mL
D.在20mL5.0mol/L CuSO4溶液中加入80mL水
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省贵阳市新天学校高一上学期期中测试化学试卷(解析版) 题型:选择题
分离碘水溶液的方法正确的是
A.蒸馏 B.萃取和分液 C.过滤 D.分液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省襄阳市四校高二上学期期中联考化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A.常温下,10mL0.02 mol•L?1 HCl溶液与10mL0.02 mol•L?1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=11
B.在0.1 mol•L?1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
C.中和物质的量浓度与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.配制三氯化铁溶液时应将三氯化铁溶于浓盐酸,再加水稀释至所需浓度
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一上学期9月教学质检化学试卷(解析版) 题型:选择题
将NO2、NH3、O2混合气22.4L通过稀硫酸后,溶液质量增加了26.7g,气体体积缩小为4.48L。(气体体积均在标况下测定)剩余气体能使带火星的木条着火,则混合气体的平均相对分子质量为(4NO2+O2+2H2O=4HNO3)
A.28.1 B.30.2 C.33.1 D.34.0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二上学期期中测试化学试卷(解析版) 题型:填空题
在100℃时,将0.200 mol的四氧化二氮气体充入2L抽空的密闭容器中,每隔一定时间对该容器内的物质进行分析,得到如下表格:
时间 | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)该反应的化学方程式为_________________,达到平衡时四氧化二氮的转化率为________%。
(2)20s时四氧化二氮的浓度c1=________mol·L-1,在0~20s时间段内,四氧化二氮的平均反应速率为________mol•L-1•s-1。
(3)若在相同情况下最初向容器中充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的初始浓度为________mol•L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com