
���� ȡ��������Һ����BaCl2��Һ�а�ɫ�������ɣ��ټ�������������������ܽ⣬�����������ɣ�˵����ɫ����ΪBaCO3��BaSO4������һ����4.3g������Һ�к���CO32-��SO42-��������м�����������ᣬ��2.33g�������ܣ������ᱵ��������2.33g��������������ӵ����ʵ�����$\frac{2.33g}{233g/mol}$=0.01mol������̼�ᱵ��������4.3g-2.33g=1.97g��̼������ӵ����ʵ�����$\frac{1.97g}{197g/mol}$=0.01mol��
����ٵ���Һ�м���������NaOH��Һ�����ȣ�������ʹʪ���ɫʯ����ֽ�����������ǰ��������ʵ�����$\frac{1.12L}{22.4L/mol}$=0.05mol��˵����Һ����NH4+�����ʵ�����0.05mol���Դ˽����⣮
��� �⣺��1�������Ϸ�����֪n��CO32-��=0.01mol��c��CO32-��=$\frac{0.01mol}{0.2L}$=0.05mol/L��
n��NH4+��=0.05mol��c��NH4+��=$\frac{0.05mol}{0.2L}$=0.25mol/L��
�ʴ�Ϊ��0.05��0.25��
��2��������Һ������ԭ����ôn��+��=n��-������ȷ��NH4+����0.05��2��0.01+2��0.01����һ������Cl-����n��Cl-��=0.01���纬�������ӡ������ӵȣ������0.01��
�ʴ�Ϊ��Cl-����0.01mol��
���� ���⿼�鳣�����ӵļ��鷽����Ϊ�߿��������ͺ�Ƶ���㣬��Ŀ�Ѷ��еȣ�ע�����ճ������ӵĻ�ѧ���ʼ����鷽������ȷ���������Ƿ����ʱ���ų��������ӣ�ȷ�����鷽���������ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������֬������������ˮ�⣬�����������ͺͷ��� | |
| B�� | �ϳ���ά��������άͳ�ƻ�ѧ��ά | |
| C�� | ����ʽΪC3H8��C6H14�������л���һ����Ϊͬϵ�� | |
| D�� | ���ۡ������ʺ���֬�����ڸ߷��ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȼ���еĽ��������Ի���̬��ʽ���ڵ� | |
| B�� | ���������Ȼ��ͬ����ұ����������ͬ�� | |
| C�� | ����������Դ�ḻ�ҿ��������ɾ����������� | |
| D�� | ������ұ�����ǰѽ��������ﻹԭΪ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ZԪ�����Ԫ��λ��ͬһ���� | |
| B�� | ������ZͶ��H2O��Ҳ�����ɻ�����W | |
| C�� | Y���ʲ�������Z2S������Ӧ | |
| D�� | XԪ�ص����к����ж����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2S2O3 ��aq��+2HCl��aq��=2NaCl��aq��+S��s��+SO2��g��+H2O��l���ڼ��������»�ѧ��Ӧ�����������Ҫԭ���Ǹ÷�Ӧ�����ȷ�Ӧ������ʹƽ�������� Ӧ�����ƶ� | |
| B�� | ���ں��������з�����Ӧ��N2��g��+3H2��g��?2NH3 ��g�����ﵽƽ����ٳ�������He������ѹǿ����ѧƽ��������Ӧ�����ƶ� | |
| C�� | �ںϳɰ���Ӧ�У�����������ͬʱ�����д���ʱ��a��������ʱ��b��������һʱ��ͼ�����ͼһ��ʾ | |
| D�� | ���ں�ѹ�����з�����Ӧ��2SO3 ��g��?2SO2 ��g��+O2 ��g�����ﵽƽ����ٳ�������He��������һʱ��ͼ�����ͼ����ʾ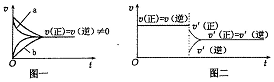 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ�������ڱҵı��棬�۲����� | B�� | ��Ӳ�� | ||
| C�� | ����ϡ���ᣬ�۲����� | D�� | ���ֵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���ᷴӦ2Fe+6H+�T2Fe3++3H2�� | |
| B�� | ̼�������Һ�м�������Ca��HCO3��2+2HCl�TCaCl2+H2O+CO2�� | |
| C�� | CO2ͨ������ʯ��ˮ��CO2+Ca2++2OH-�TCaCO3��+H2O | |
| D�� | NaHCO3��Һ�м�������HCO3-+H+�TH2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | H2SO4 | C�� | NaOH��Һ | D�� | HNO3��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com