
ƻ������һ����ƻ�����Ͷ��γɵľ��нⶾ����֬�����ʵ�����ҩЧ�Ľ���ʳƷ��ƻ����(2?�ǻ�������)���������ϵ���Ҫ�������ʣ�ƻ����Ľṹ��ʽΪ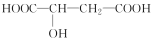 ���������˵������ȷ����
���������˵������ȷ����
A��ƻ������һ���������ܷ���������Ӧ
B��ƻ������һ���������ܷ�����������Ӧ
C��1 molƻ����������Na��Ӧ����33.6 L H2(��״����)
D��1 molƻ������Na2CO3��Һ��Ӧһ������2 mol Na2CO3
 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ��һ��ѧ����ѧ�Ծ��������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�����,����������ȷ����
A����״����,2��24 L Cl2ͨ������NaOH��Һ��,��Ӧת�Ƶ��ӵ���ĿΪ0��2NA
B��1 mol K������O2��Ӧ,����K2O��K2O2��KO2�Ļ����ʱת�Ƶĵ�����ΪNA
C�����³�ѹ��,1��7 g H2O2�к��еĵ�����ΪNA
D����״����,1 mol CO2�������õ��Ӷ���Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����Ļ�������������һ�и�����ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���м����ǩ����ʴ���Լ���Al2(SO4)3��Һ��KOH��Һ��NaAlO2��Һ ��H2SO4��Һ��NaHCO3��Һ�� HCl��Һ��AgNO3 ����ˮ��CuSO4��Һ��NaOH��Һ��CCl4��NaCl��Һ�����������Լ���ֻ�ý�ͷ�ιܺ��ԹܾͿ��Լ������
A ���٢ڢۢ� B���٢ڢܢݢ� C���٢ڢۢܢ� D��ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z��W��R��5�ֶ�����Ԫ�أ���ԭ��������������X�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�������������Ǵ�����������3����R��Y����ͬһ���壬Z�Ƕ������н�������ǿ�Ľ���Ԫ�أ� W������������Ӧˮ��������Z��R������������Ӧˮ�������Ӧ�����κ�ˮ������˵����ȷ����
A��Ԫ��Y��Z��W���Ӿ�����ͬ�ĵ��Ӳ�ṹ����뾶��������
B��Ԫ��X��Ԫ��Y���γ����ֻ�ѧ��������ȫ��ͬ�Ļ�����
C��Ԫ��Y��R�ֱ���Ԫ��X�γɵĻ���������ȶ��ԣ� XmY>XmR
D��Ԫ��X��Z�γɻ�����ĵ���ʽ���Ա�ʾ��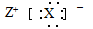
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ����У������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
���г��������Լ��Ͳ�������������
ѡ�� | ���ʣ�������Ϊ���ʣ� | �����Լ� | ���� |
A | CO2��SO2�� | ����NaHCO3��Һ | ϴ�� |
B | BaCO3��BaSO4�� | ����Na2CO3��Һ | ���衢���� |
C | �������ӣ� | Ũ��ˮ | ���� |
D | Cl2��HCl�� | ����ʳ��ˮ | ϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�߶��ϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z��WΪ���ֶ���������Ԫ�أ�����X��Zͬ�壬Y��Zͬ���ڣ�W�Ƕ���������Ԫ����ԭ�Ӱ뾶���ģ�Xԭ�������������Ǻ�����Ӳ�����3����Y���������������۴�����Ϊ6������˵����ȷ����
A��YԪ������������Ӧ��ˮ���ﻯѧʽH2YO4
B��ԭ�Ӱ뾶�ɴ�С��˳��Ϊ��Z��Y�� W
C��X��Z����Ԫ�ص���̬�⻯���У�Z����̬�⻯����ȶ�
D��X��W�γɵ����ֻ������У��������������ʵ���֮�Ⱦ�Ϊ1�U2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������������ѧ�߶���9�¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
25�棬101kPaʱ��ʹ1.0 g��������������Ӧ�������Ȼ��ƾ��岢�ų�17.87kJ������������1 mol NaCl�ķ�Ӧ��Ϊ
A��17.87kJ B����17.87kJ/mol
C��411 kJ/mol D����411 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�л���ķ���ʽΪCxHyO2������������������Ϊ20.25%��̼����������Ϊ68.35%�������������£���ˮ�������Һͱ������л������ͬ�¶Ⱥ�ѹǿ�£�ͬ�������Һͱ���������ռ�������ͬ����Ľṹ������
A��18�� B��16�� C��14�� D��8��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ��ɽ�и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��10�֣�����β���dz��п�������Ҫ��Ⱦ���μ�������β��(CO��NOx��)����Ⱦ����Ҫ�Ŀ�ѧ�о����⡣
��1����֪��N2(g) + O2(g) 2NO(g) ��H1
2NO(g) ��H1
N2(g) + 3H2(g) 2NH3(g) ��H2
2NH3(g) ��H2
2H2(g) + O2(g) 2H2O(g) ��H3
2H2O(g) ��H3
��4NO(g) + 4NH3(g) + O2(g) 4N2(g) + 6H2O(g) ��H =____________(�æ�H1����H2����H3����)
4N2(g) + 6H2O(g) ��H =____________(�æ�H1����H2����H3����)
��2�����ܱ������У�һ�������£��������·�Ӧ��2NO(g)��2CO(g) N2(g)��2CO2(g)������˵������˵���÷�Ӧ�ﵽƽ�����__________ (����ĸ)
N2(g)��2CO2(g)������˵������˵���÷�Ӧ�ﵽƽ�����__________ (����ĸ)
A��NO������������NO�������������
B��v(CO)=v(CO2)
C����ϵ��ѹǿ���ֲ���
D�������ʵ�Ũ�ȱ��ֲ���
��3�����û���̿��ԭ��������������йط�Ӧ�Ļ�ѧ����ʽΪ��
C(s) + 2NO(g) N2(g) + CO2(g) ��H >0
N2(g) + CO2(g) ��H >0
ij�о�С�����ܱ���������һ�����Ļ���̿��NO������(T1��)�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
Ũ��/mol��L-1
| NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
��д���÷�Ӧ��ƽ�ⳣ������ʽ��K= ��
��30 min�ı�ijһ������ƽ�ⷢ�����ƶ�����ı�������� ��
�������¶ȣ�NOŨ�Ƚ� ������������䡱��С������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com