
【题目】F(4-苯并呋喃乙酸)是合成神经保护剂依那朵林的中间体,某种合成路线如下:
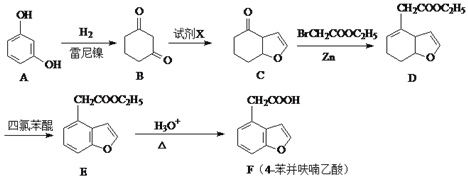
(1)化合物F中的含氧官能团为_________和___________(填官能团的名称)
(2)试剂X分子式为C2H3OCl,分子中既无甲基也无环状结构且可发生银镜反应,则X的结构简式为__________;由E→F的反应类型为___________。
(3)写出同时满足下列条件的E的一种同分异构体的结构简式____________。
Ⅰ. 能发生银镜反应 Ⅱ. 分子中含有1个苯环且有3种不同化学环境的氢
(4)借鉴由C到D的合成机理,请写出以![]() 和BrCH2COOC2H5为原料制备
和BrCH2COOC2H5为原料制备![]() 的合成路线流程图(无机试剂可任选)_____。
的合成路线流程图(无机试剂可任选)_____。
合成路线流程图示例如下:CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
【答案】 羧基 醚键 ClCH2CHO 取代(水解)反应 

【解析】(1)由F的结构可知,含有的含氧官能团为羧基、醚键;
(2)试剂X分子式为C2H3OCl,且分子中既无甲基也无环状结构,则X的结构简式为ClCH2CHO;由E→F发生酯的水解反应,属于取代反应;
(3)E的一种同分异构体满足:Ⅰ.能发生银镜反应,含有醛基,Ⅱ.分子中含有1个苯环且有3种不同化学环境的氢,可以含有3个-CH2CHO,且处于间位位置,结构简式为 等;
等;
(4)![]() 与HBr发生加成反应得到
与HBr发生加成反应得到![]() ,在氢氧化钠水溶液、加热条件下水解生成
,在氢氧化钠水溶液、加热条件下水解生成![]() ,发生催化氧化生成
,发生催化氧化生成![]() ,结合转化关系中C→D反应,
,结合转化关系中C→D反应,![]() 与BrCH2COOC2H5/Zn作用得到
与BrCH2COOC2H5/Zn作用得到 ,最后再酸性条件下水解得到
,最后再酸性条件下水解得到![]() ,合成路线流程图:
,合成路线流程图: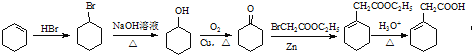 。
。


科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(S)+CO(g)![]() MgO(S)+CO2(g)+SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
MgO(S)+CO2(g)+SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )

选项 | x | y |
A | SO2的浓度 | 平衡常数K |
B | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
D | MgSO4的质量(忽略体积) | CO的转化率 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组将一批电子废弃物简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计如下制备硫酸铜晶体和无水氯化铁的方案:
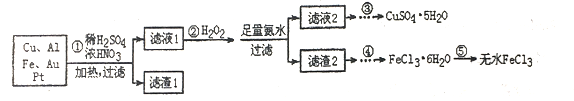
已知:Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O
请回答下列问题:
(1)步骤①Cu与酸反应的离子方程式为_________________________。
(2)步骤②加H2O2的作用是______________,滤渣2为(填化学式)__________。
(3)步骤⑤不能直接加热脱水的理由是________
(4)若滤液1中Cu2+的浓度为0.02mol·L-1,则氢氧化铜开始沉淀时的pH=________(已知:Ksp[Cu(OH)2]=2.0x10-20)
(5)已知:2Cu2++4I-=2CuI↓+I2 I2+2S2O32-=2I-+S4O62-
某同学为了测定CuSO4·5H2O产品的质量分数可按如下方法:取3.00g产品,用水溶解后,加入足量的KI溶液,充分反应后过滤、洗涤,将滤液稀释至250mL,取50mL加入淀粉溶液作指示剂,用0.080mol·L-1Na2S2O3标准溶液滴定,达到滴定终点的依据是______________。
四次平行实验耗去Na2S2O3标准溶液数据如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
此产品中CuSO4·5H2O的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法不正确的是( )
A. 常温常压下,2 g D2O 中含中子数为NA
B. 标况下,22.4L 己烷中碳原子数为6NA
C. 2.4g Mg 在空气中充分燃烧,转移的电子数为0.2NA
D. 28g乙烯和丙烯(C3H6)的混合气体含有的碳氢键数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列化学方程式或离子方程式。
(1)工业用电解饱和食盐水制氯气的化学方程式为____________________。
(2)向新制的Na2S 溶液中滴加新制的氯水的离子方程式为_______________。
(3)氯化铝与过量NaOH 溶液反应的离子方程式为____________________。
(4)乙醇催化氧化制乙醛的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是重要的有机化工原料,也是优质的燃料,工业上可由乙烯水合法或发酵法生产。回答下列问题:
(1)乙烯水合法可分为两步
第一步:反应CH2=CH2+ HOSO3H(浓硫酸)→CH3CH2OSO3H(硫酸氢乙醋);
第二步:硫酸氢乙酯水解生成乙醇。
① 第一步属于反应____________________(填反应类型)。
② 第二步反应的化学方程式为__________________________________。
③ 上述整个过程中浓硫酸的作用是___________________________________。
(2)发酵法制乙醇,植物秸秆(含50%纤维素)为原料经以下转化制得乙醇
植物秸秆—水解→C6H12O6—酒化酶→2CH3CH2OH+2CO2↑
![]()
纤维素的化学式为_______________,现要制取4.6 吨乙醇,至少需要植物秸秆________吨。
(3)乙醇汽油是用90%的普通汽油与10 %的燃料乙醇调和而成。乙醇汽油中乙醇是可再生能源,来源于_______________(填“乙烯水合法”或“发酵法”)。
(4)以乙醇为原料可制备某种高分子涂料,其转化关系如下图:

① 有机物A 的结构简式为____________。
② 反应Ⅱ的化学方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料。工业上利用下列反应来检查氯气管道是否漏气:3Cl2+8NH3=N2+6NH4Cl,下列说法错误的是
A. 若有白烟产生则管道漏气 B. 该反应中NH4Cl是还原产物
C. 反应中NH3只显还原性 D. 生成1.4gN2时转移0.3mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素。X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。N是用量最多的金属元素。下列说法不正确的是

A. 原子半径:W>Y>Z>M>X
B. N的一种氧化物可用作油漆和涂料
C. 热稳定性:XM>X2Z
D. X2Z、WM4分子中各原子最外层均为8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. H2SO4溶液与氨水反应:H++OH-===H2O
B. CuO与稀盐酸反应:CuO+2H+===Cu2++H2O
C. AlCl3溶液与氢氧化钠溶液反应:AlCl3+3OH-===Al(OH)3↓+3Cl-
D. Cl2与氢氧化钠溶液反应:Cl2+2OH-===2ClO-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com