
| A、在1 L 0.2 mol?L-1的Na2CO3溶液中含有CO32-的数目为0.2NA |
| B、0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.3 NA |
| C、15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.2NA |
| D、1 mol Na2O2中含有的阴离子数目为2NA |
| 15.6g |
| 78g/mol |


科目:高中化学 来源: 题型:
| A、S2-水解反应:S2-+2H2O?H2S+2OH- |
| B、氯气与氯化亚铁溶液反应:Cl2+2Fe2+═2Fe3++2Cl- |
| C、H2CO3在水中电离:H2CO3?2H++CO32- |
| D、氢氧化钠溶液吸收过量的二氧化碳:2NaOH+CO2═Na2CO3+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑤ | B、①④⑥ |
| C、①②④⑥ | D、①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第ⅠA碱金属元素与ⅦA元素所形成的化合物在固态时为离子晶体,晶体中阴阳离子排列方式相同 |
| B、晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子 |
| C、离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键 |
D、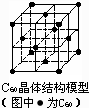 C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有12个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PbO2具有氧化性 |
| B、白色不溶物为PbSO3 |
| C、白色不溶物为PbSO4 |
| D、白色不溶物既是氧化产物又是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、提倡作物秸秆就地焚烧 |
| B、加强城市生活污水脱氮除磷处理,遏制水体富营养化 |
| C、积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用 |
| D、大力实施矿物燃料“脱硫、脱硝技术”,减少硫氧化物和氮氧化物的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| B、由于Fe可被浓H2SO4氧化,因此常温下不能用钢瓶贮浓H2SO4 |
| C、镁铝合金的熔点比镁和铝都高 |
| D、不能用氨水鉴别Al3+﹑Mg2+﹑Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.6mol/L |
| B、0.06mol/(L?s) |
| C、0.03mol/L |
| D、0.03mol/(L?s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com