
下列说法正确的是 ( )
A.苯和乙烯都能使溴水退色,其褪色原理是相同的
B.所有烷烃和蛋白质分子中都存在碳碳单键
C.人们通常用聚乙烯、聚氯乙烯塑料来制食品包装袋,它们都是高分子化合物
D.乙醇可以转化成乙酸,乙醇和乙酸都能发生取代反应
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)具有很强的氧化性,是一种新型的高效水处理剂。
(1)高铁酸钾具有强氧化性的原因是 。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为 ,___ _____。
(3)制备K2FeO4可以采用干式氧化法或湿式氧化法。
① 干式氧化的初始反应是2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中每生成2 mol Na2FeO4时转移电子 mol。
② 湿式氧化法的流程如下图:
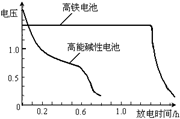
上述流程中制备Na2FeO4的化学方程式是 。
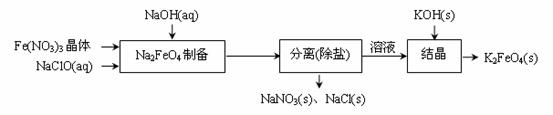
(4)高铁电池是正在研制中的可充电电池,右图为该电池和常用的高能
碱性电池的放电曲线,由此可得出的高铁电池的优点有 、
。
(5)探究高铁酸钾的某种性质。
【实验1】将适量K2FeO4固体分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0 mmol·L-1(1 mmol·L—1 =10—3 mol·L—1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。
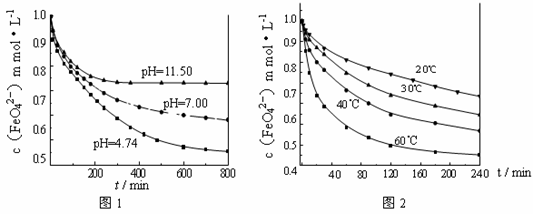
【实验2】将适量 K2FeO4 溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为
1.0 mmol·L-1 的试样,将试样分别置于 20℃、30℃、40℃和60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
①实验1的目的是 ;
②实验2可得出的结论是 ;
③高铁酸钾在水中的反应为4 FeO42—+10 H2O 4 Fe(OH)3 +8OH—+3 O2↑。 由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
4 Fe(OH)3 +8OH—+3 O2↑。 由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定中和反应的反应热,计算时至少需要的数据是
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量 ⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
A.①②③⑥ B.①③④⑥
C.③④⑤⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法正确的是
A.金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti
B. 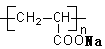 表示一种吸水性高分子树脂
表示一种吸水性高分子树脂
C.用于现代建筑的钢筋混凝土不属于复合材料
D.山东东营广饶县一男子收到网购物品后,因吸入氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构
简式为FCH2COOCH3,能与H2发生加成反应,也能被LiAlH4还原
查看答案和解析>>
科目:高中化学 来源: 题型:
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如下图:
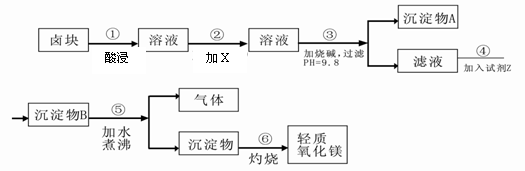
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH 表2 化学试剂价格表
| 试剂 | 价格(元/吨) |
| 漂液(含NaClO,25.2%) | 450 |
| 双氧水(含H2O2 ,30%) | 2400 |
| 烧碱(含98% NaOH) | 2100 |
| 纯碱(含99.5% Na2CO3) | 600 |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
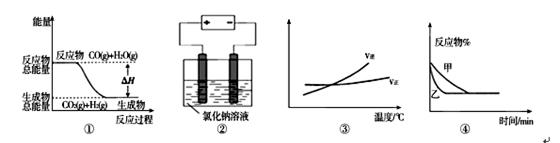
关于下列四个图象的说法中正确的是 ( )
A.图①表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0
CO2(g)+H2(g)”中的△H大于0
B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1
C.图③表示可逆反应“A2(g)+3B2(g) 2AB3(g)”的△H小于0
2AB3(g)”的△H小于0
D.图④表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知物质A是芳香族化合物,A分子中苯环上有2个取代基,均不含支链且A的核磁共振氢谱有6个吸收峰,峰面积比为1:1:1:1:2:2,能够与FeCl3溶液发生显色反应。D分子中除含2个苯环外还含有1个六元环。它们的转化关系如下:

请回答下列问题:
(1)A中所含官能团的名称为 。
(2)反应①~③属于加成反应的有 (填序号)。
(3)B的结构简式 ,D的结构简式 。
(4)A→E的化学方程式为 。
(5)符合下列条件的A的同分异构体有 种。
①芳香族化合物,苯环上的取代基不超过3个;
②能与FeCl3溶液发生显色反应且不能水解;
③lmol该物质可与4mol﹝Ag(NH3)2﹞+发生银镜反应;
④lmol该物质可与5molH2加成。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于可逆反应的叙述正确的是:
A.可逆反应是指既能向正反应方向进行,同时又能向逆反应方向进行的反应
B.2H2O 2H2+O2与2H2+O2
2H2+O2与2H2+O2 2H2O互为可逆反应
2H2O互为可逆反应
C.对于可逆反应,当正反应速率增大时,逆反应速率就会减小
D.外界条件对可逆反应的正、逆反应速率影响的程度不一定相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com